杜仲片质量标准研究
林向前
(福建省漳州市中医院,福建 漳州 363000)
杜仲片是我院骨伤科经典传统中药制剂,可补肾强腰、活血化瘀,适用于急慢性腰部损伤、关节酸痛等肾虚血瘀证,50多年的临床应用证明,该药疗效确切且未见不良反应[1]。为控制其质量,笔者参考文献[2],建立了杜仲片的质量标准。现报道如下。
1 仪器与试药
仪器:Agilent 1260型高效液相色谱仪,包括Agilent-G1311C型四元泵,Agilent G1329B型真空脱气器,Agilent-G1315D型二极管阵列检测器,Chemstation B.04.02型化学工作站[3](美国安捷伦公司);KQ-250B 型超声清洗机(昆山超声仪器有限公司);Mettler Toledo EL2401型电子天平(瑞士梅特勒-托利多公司)。
试药:芍药苷对照品(批号为 110736-201136,含量以96.0%计,使用前无需处理),当归对照药材(批号为 927-200110),丹皮酚对照品(批号为 0708-9704),延胡索乙素对照品(批号为0726-200208),均购自中国食品药品检定研究院;杜仲片(批号分别为20150701,20150901,20151101),杜仲片缺味阴性对照品,均由本院制剂中心提供;乙腈为色谱纯,水为重蒸馏水,其他试剂均为分析纯。
2 方法与结果
2.1 一般质量控制
性状:本品为褐黑色片;气微辛,味微苦。
检查:按2015年版《中国药典(四部)》通则0101片剂项下有关规定,对3批样品重量差异、崩解时限、微生物限度进行检查,结果均符合规定[4]。
2.2 定性鉴别
当归:取杜仲片20片,捣碎成细粉,加乙醚40 mL,超声处理5 min,静置2 h,滤过,滤液蒸发干燥,干燥物加入乙酸乙酯1 mL,充分搅拌使其溶解,作为供试品溶液。另取当归对照药材1 g,按上述方法制备对照药材溶液[5]。同法制备缺当归的阴性对照品溶液。按2015年版《中国药典(四部)》通则0502薄层色谱法[4]试验,吸取上述3种溶液各6 μL,分别点于同一硅胶G薄层板上,以石油醚(60~90℃)-乙酸乙酯(50∶1)为展开剂,展开,取出,晾干,置紫外光灯(365 nm)下检视[6]。供试品溶液色谱中,在与对照药材溶液色谱相应位置上显相同颜色的荧光斑点,阴性对照无干扰(图1 A)。
牡丹皮:取当归鉴别项下的供试品溶液,作为供试品溶液。另取丹皮酚对照品,加乙酸乙酯制成每1 mL含1 mg的溶液,作为对照品溶液。同法制备缺牡丹皮饮片的阴性对照品溶液[5]。照2015年版《中国药典(四部)》通则0502薄层色谱法[4]试验,吸取上述3种溶液各8 μL,分别点于同一硅胶G薄层板上,以环己烷-乙酸乙酯-冰醋酸(10 ∶1 ∶0.1)为展开剂,展开,取出,晾干,置紫外光灯(254 nm)下检视[6]。供试品溶液色谱中,在与对照品溶液色谱相应位置上显相同颜色的荧光斑点,阴性对照无干扰(图1 B)。
延胡索:取杜仲片30片,捣碎成细粉,加甲醇50 mL,超声处理20 min,滤过,滤液蒸发干燥,干燥物加水15 mL搅拌使其溶解,用氨水调pH至9~10,用乙醚提取2次,每次15 mL,合并乙醚液,挥干,残渣加乙酸乙酯1 mL充分搅拌使溶解,作为供试品溶液[5]。另取延胡索乙素对照品,加甲醇制成每1 mL含1 mg的溶液,作为对照品溶液。同法制备缺醋延胡索饮片的阴性对照品溶液。照2015年版《中国药典(四部)》通则0502薄层色谱法[4]试验,吸取上述3种溶液各8 μL,分别点于同一硅胶 G 薄层板上,以正己烷 - 氯仿 - 甲醇(7.5∶4∶1)为展开剂,展开,取出,晾干,置碘蒸气熏至斑点显色清晰,在空气中挥尽板上吸附的碘后,置紫外光灯(365 nm)下检视[6]。供试品溶液色谱中,在与对照品溶液色谱相应位置上显相同颜色的荧光斑点,阴性对照无干扰(图1 C)。

图1 杜仲片薄层色谱图
2.3 芍药苷含量测定
2.3.1 色谱条件及系统适用性试验
色谱柱:Lichrospher-C18柱(250 mm ×4.6 mm,5 μm);流动相:乙腈 - 0.1% 磷酸溶液(13 ∶87);流速:1.0 mL /min;检测波长:230 nm;柱温:30 ℃ ;进样量:10 μL。在此色谱条件下,芍药苷达到基线分离(芍药苷色谱峰与相邻色谱峰之间的分离度大于1.50)[7],理论板数按芍药苷峰计应不低于2 000,详见图2。
2.3.2 溶液制备
取杜仲片10片,捣碎成细粉,称取约0.5 g,精密称定,放入带有瓶塞的锥形瓶中,加入70%甲醇50 mL,盖紧瓶塞,准确称定总质量,超声处理(功率250 W,频率50 kHz)30 min,放冷,再称定质量,用上述溶剂补足减失的质量,摇匀,滤过,取续滤液,即得供试品溶液[8-9]。同法制得缺赤芍、牡丹皮的阴性对照品溶液。取芍药苷对照品适量,精密称定,加甲醇制成含芍药苷0.12 g/L的溶液,摇匀,即得对照品溶液。
2.3.3 方法学考察[2]
专属性试验:按2.3.1项下色谱条件,分别精密量取对照品溶液、供试品溶液和阴性对照品溶液各10 μL,注入液相色谱仪,测定,记录色谱图(图2)。结果供试品溶液色谱中,在与对照品溶液色谱相同位置上有相同时间保留峰,而阴性对照无干扰。芍药苷保留时间约为20.8 min,测得理论板数按芍药苷峰计为14 506。
线性关系考察:分别精密吸取对照品溶液(117.408μg/mL)1,2,4,6,8,10 μL,注入液相色谱仪,按拟订色谱条件进样测定,以峰面积积分值(Y)为纵坐标、芍药苷进样量(μg,X)为横坐标绘制标准曲线,得回归方程Y = 1 242.638 8 X -7.596 3,r=0.999 8(n=6)。结果表明,芍药苷进样量在 0.117 408 ~ 1.174 080 μg 范围内与峰面积积分值线性关系良好。
精密度试验:精密吸取同一对照品溶液(117.408μg/mL)5 μL,重复进样 6次。结果峰面积积分值的 RSD为0.19%(n=6),表明仪器精密度良好。
重复性试验:取同一批(批号为20150701)供试品6份,依法制备供试品溶液(定容至50 mL具塞锥形瓶中),按拟订色谱条件进样,以芍药苷峰面积积分值计算含量。结果见表1,可见,方法重复性良好。

图2 杜仲片高效液相色谱图

表1 重复性试验结果(n=6)
稳定性试验:取同一供试品溶液,注入液相色谱仪,分别于 0,2,4,8,12,16 h 时依法测定峰面积[10]。结果分别为 838.239 38,839.581 48,837.495 97,839.503 11,840.758 06,840.421 88,RSD 为 0.15% (n =6),表明供试品溶液在16 h内稳定。
加样回收试验:精密量取已知含量(批号为20150701,含量为 6.48 mg /g)的样品 0.25 g,置 25 mL具塞锥形瓶中,分别精密加入芍药苷对照品适量,按拟订方法制备供试品溶液并测定。结果见表2。
2.3.4 样品含量测定
精密称取3批杜仲片,按拟订方法制备供试品溶液,依法测定芍药苷含量。结果批号为 20150701,20150901,20151101的3批样品中芍药苷含量分别为6.48,6.37,6.57 mg /g,平均含量为 6.473 mg /g。
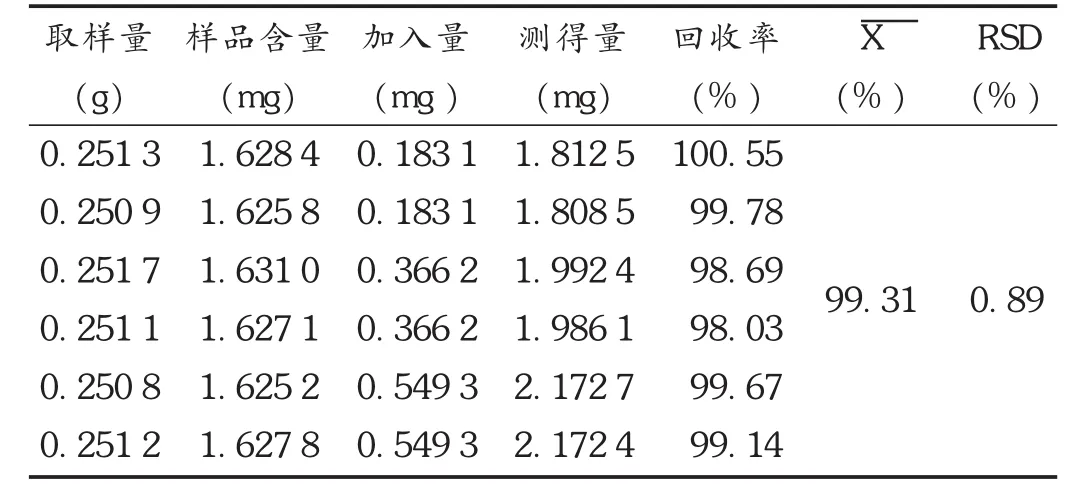
表2 芍药苷加样回收试验结果(n=6)
3 讨论
3.1 定性指标选择
杜仲为杜仲片的君药,松脂醇二葡萄糖苷为杜仲的主要有效成分,参考2015年版《中国药典(一部)》的方法,色谱柱采用 Lichrospher-C18柱(250 mm ×4.6 mm,5 μm),流动相为乙腈 - 0.1% 磷酸溶液(13 ∶87),检测波长为 227 nm,进样量为10 μL,柱温为30℃,对杜仲片中的松脂醇二葡萄糖苷进行测定,结果供试品溶液及阴性对照品溶液在与松脂醇二葡萄糖苷相同保留时间处均未检出色谱峰,说明样品中含量甚微,这可能与盐杜仲的加热炮制及杜仲片的生产工艺有关,故暂不建立杜仲片中松脂醇二葡萄糖苷的含量测定方法。
3.2 提取溶剂选择
取杜仲片10片,捣碎成细粉,称取约0.5 g,精密称定,置具塞锥形瓶中,分别精密加入稀乙醇、70%甲醇、甲醇各50 mL,密塞,称定质量,超声处理(功率250 W,频率50 kHz)30 min,放冷,再称定质量,用上述溶剂补足减失的质量,摇匀,滤过,取续滤液,即得供试品溶液。结果用稀乙醇、70%甲醇、甲醇提取得芍药苷含量分别为 4.02,6.57,5.16 mg /g。可见,采用 70% 甲醇作为提取溶剂,样品中芍药苷的含量明显较高。
3.3 赤芍薄层鉴别
由于处方中赤芍饮片具有散瘀止痛的功效,故本研究中曾尝试进行赤芍的薄层鉴别,分别采用多种提取方法(①正丁醇直接提取;②正丁醇直接提取后用氨试液洗涤;③正丁醇直接提取后用氨试液洗涤,取正丁醇层再用水洗涤等),并进行比较,最后选用背景干扰较少的方法③进行提取,阴性对照品溶液的制备方法同③。对提取液采用2种展开系统[氯仿-甲醇-醋酸乙酯(8∶3∶1)氨饱和 20 min,以及氯仿 -醋酸乙酯 -甲醇 -甲酸(40 ∶5 ∶10 ∶0.2)]进行展开鉴别,发现缺赤芍的阴性对照品溶液均有干扰,故不对此进行鉴别。
3.4 显微鉴别
试验中还曾尝试进行杜仲的显微鉴别,但由于投料加工后受其他药材染色的影响,色较暗,与投料用的盐杜仲在特征上虽有一定差异,但很难观察。此外,杜仲药材所具有的石细胞显微特征,在制剂中并不具唯一性。因此,不对杜仲进行显微鉴别。
[1]林向前 .杜仲片提取工艺研究[J].中国药业,2013,22(13):32-33.
[2]邵红燕,张和明,刘志海.骨质增生贴质量标准研究[J].中国药房,2010,21(27):2563 - 2564.
[3]王丽聪,李 松.苦参配方颗粒质量控制研究[J].现代药物与临床,2012,27(5):471 - 473.
[4]国家药典委员会.中华人民共和国药典(四部)[M].北京:中国医药科技出版社,2015:3 -4,57-59.
[5]杨 艳,郝丽晓,李利芬,等.对中药材市场丹参质量的考察[J].科技情报开发与经济,2004,14(2):125 - 126.
[6]夏 荃.祛斑胶囊质量控制方法的研究[J].陕西中医学院学报,2006,29(2):64 - 65.
[7]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2015:105.
[8]杨 培,李 建,徐 蓓,等.黔产山银花栽培品种的鉴定与含量测定[J].中国药业,2007,16(16):20 - 21.
[9]刘会前,李成网.十四味连黄烧伤软膏的制备与质量控制[J].中国医院药学杂志,2009,29(16):1401 - 1403.
[10]李 虹.肾石通颗粒质量标准的研究[J].中国药品标准,2010,11(3):176 - 179.

