夜间加餐营养支持对慢加急性肝衰竭患者TIPS治疗后的影响
徐晓萌 张盼盼 宋佳 原翔
河南科技大学第一附属医院肿瘤内科,洛阳 471000
慢加急性肝衰竭是一种因急性损伤作用导致肝功能相对稳定慢性肝病患者病情迅速恶化的肝衰竭综合征,临床上通过经颈静脉肝内门体静脉分流术(transju-gular intrahepatic portosystemic shunt,TIPS)以控制肝衰竭患者急性失代偿事件的发生[1-6]。但TIPS治疗后的慢加急性肝衰竭患者因肝功能减退,从而导致物质代谢失衡,增加营养不良的发生风险[7]。相关研究显示,60%以上的慢加急性肝衰竭患者存在营养不良状况,主要由于患者疾病急性发作期间出现饮食摄入不足、营养吸收障碍、营养物质代谢紊乱等多种情况所致[8]。营养支持治疗可以一定程度上增强患者的营养吸收,是肝衰竭患者需采取的必要干预手段[9-10]。根据肝衰竭患者夜间的物质代谢特点,本研究考虑在常规的日间营养干预治疗上进行夜间加餐,进一步分析其对肝衰竭患者营养状况各方面的作用[11]。
资料与方法
1.一般资料
前瞻性研究,选取2020年9月至2022年9月来河南科技大学第一附属医院接受治疗的107例经TIPS治疗后的慢加急性肝衰竭患者,根据简单随机化法将其分为对照组(53例)与研究组(54例)。研究组:男45例,女9例,年龄24~67(52.48±5.02)岁。对照组:男42例,女11例,年龄27~69(53.15±4.79)岁。两组患者一般资料比较,差异均无统计学意义(均P>0.05),具有可比性。⑴纳入标准:符合慢加急性肝衰竭的诊断标准[12]并入院接受TIPS治疗;年龄18~70岁;营养风险筛查(NRS-2002)评分均≥3分,存在营养不良风险;患者及家属均知晓本研究并签署知情同意书。⑵排除标准:合并肝癌或肝性脑病;近1个月接受营养支持治疗;合并糖尿病或恶性肿瘤等消耗性疾病;哺乳期或孕期;入院时有明确感染性疾病。⑶剔除标准:因个人原因自愿退出本研究;夜间加餐次数>3次;研究过程中出现疾病恶化需进行其他治疗。
本研究经河南科技大学第一附属医院医学伦理委员会审批通过(20200918)。
2.方法
根据肝衰竭患者的具体情况,入院后均接受相应的常规药物治疗,包括利尿、护肝、对症支持治疗。
对照组患者接受日间营养支持治疗。⑴健康教育:由医生及营养师共同确定健康教育内容,包括营养不良的病因、营养摄入的必要性以及肝功能恢复的重点等知识,及时解答患者的疑惑,30 min/次,1次/周。⑵营养方案:由营养师根据患者的具体情况制定个性化的营养方案,按照营养供能标准合理安排饮食时间及日间饮食分配,为患者制定1周食谱并督促患者家属按照食谱为患者进行配餐。⑶日常饮食记录:记录患者每日的饮食情况,包括进餐次数、进餐时间、蛋白质摄入量、脂肪摄入量、碳水化合物摄入量,根据患者的饮食摄入情况及时进行调整,加强患者对各类食物营养成分的认知能力。治疗时间1个月。
研究组患者在对照组的基础上增加夜间加餐营养支持治疗,由营养师、专科医生以及护理人员共同制定加餐内容(40 g面包和100 g酸奶),于夜间21:00-22:00统一提供加餐食品,发放前需核实食物是否处在保质期内,食物是否新鲜。评估患者的夜间加餐情况,督促患者按时、按量完成加餐。加餐营养素配比情况:热量250 kcal、脂肪7.7 g、蛋白质6.7 g、碳水化合物40 g、益生菌0.78 g以及适量维生素。治疗时间1个月。
3.观察指标
⑴营养风险:治疗前1 d、治疗1周及治疗1个月,由主治医师根据NRS-2002评估患者的营养风险情况[13],得分0~7分,总评分≥3分表示存在营养不良风险。⑵肝脏储备功能:治疗前1 d、治疗1周及治疗1个月,由主治医师根据Child-Pugh肝功能分级标准[14]评估患者的肝脏储备功能,总分15分,分数越高,肝脏储备功能越差。⑶人体测量学指标:治疗前1 d及治疗1个月,由值班护士测量患者的相关人体测量指标,包括肱三头肌皮褶厚度(TSF)、体质量指数(BMI)、上臂肌围(MAMC)[15]。⑷蛋白水平:治疗前1 d及治疗1个月,采集患者静脉血以测量蛋白水平,包括白蛋白(ALB)、前白蛋白(PA)、转铁蛋白(TRF)水平[16]。
4.统计学方法
应用SPSS 25.0统计学软件进行数据处理。计数资料用率(%)表示,无序二分类资料或多分类资料采用χ2检验;符合正态分布的计量资料以均数±标准差()表示,组间比较采用独立样本t检验,组内采用配对t检验,P<0.05表示差异有统计学意义。
结果
1.两组患者营养风险比较
治疗1周后,两组患者的NRS-2002评分均高于治疗前(均P<0.05),治疗1个月后研究组的NRS-2002评分低于对照组(P<0.05),见表1。
表1 两组慢加急性肝衰竭患者营养风险比较(分,)
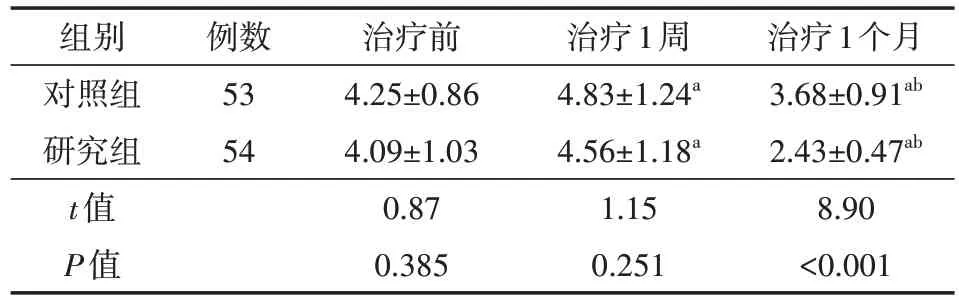
表1 两组慢加急性肝衰竭患者营养风险比较(分,)
注:对照组接受日间加餐营养支持治疗,研究组在对照组的基础上增加夜间加餐营养支持治疗;与同组治疗前比较,aP<0.05,与同组治疗1周后比较,bP<0.05
治疗1个月3.68±0.91ab 2.43±0.47ab 8.90<0.001组别对照组研究组t值P值例数53 54治疗前4.25±0.86 4.09±1.03 0.87 0.385治疗1周4.83±1.24a 4.56±1.18a 1.15 0.251
2.两组患者肝脏储备功能比较
研究组治疗1个月后的Child-Pugh评分低于对照组(P<0.05),见表2。
表2 两组慢加急性肝衰竭患者的肝脏储备功能比较(分,)

表2 两组慢加急性肝衰竭患者的肝脏储备功能比较(分,)
注:对照组接受日间加餐营养支持治疗,研究组在对照组的基础上增加夜间加餐营养支持治疗;与同组治疗前比较,aP<0.05,与同组治疗1周后比较,bP<0.05
治疗1个月8.64±1.63ab 7.12±1.41ab 5.16<0.001组别对照组研究组t值P值例数53 54治疗前10.06±2.17 9.75±1.86 0.79 0.430治疗1周9.34±1.77 8.99±2.06a 0.94 0.348
3.两组患者的人体测量学指标比较
研究组治疗1个月后BMI、MAMC、TSF水平均高于对照组(均P<0.05),见表3。
表3 两组慢加急性肝衰竭患者人体测量学指标比较()
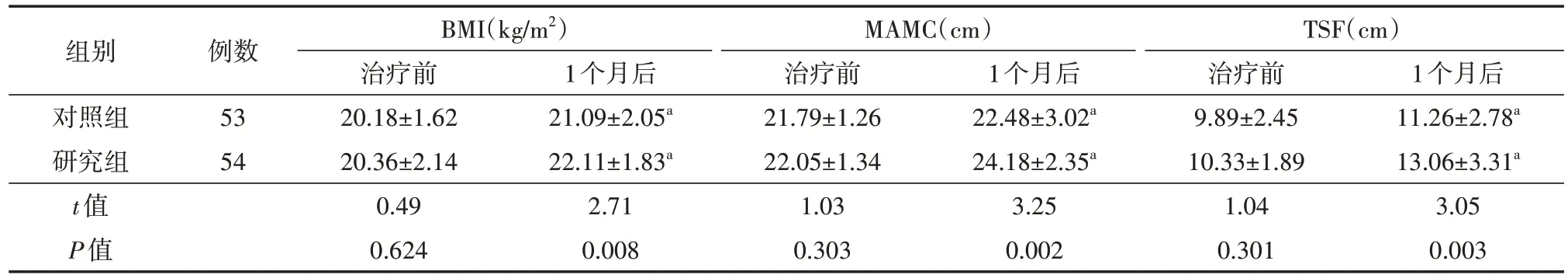
表3 两组慢加急性肝衰竭患者人体测量学指标比较()
注:对照组接受日间加餐营养支持治疗,研究组在对照组的基础上增加夜间加餐营养支持治疗;BMI为体质量指数,MAMC为肱三头肌皮褶厚度,MAMC为上臂肌围;与同组治疗前比较,aP<0.05
1个月后11.26±2.78a 13.06±3.31a 3.05 0.003组别对照组研究组t值P值例数53 54 BMI(kg/m2)治疗前20.18±1.62 20.36±2.14 0.49 0.624 1个月后21.09±2.05a 22.11±1.83a 2.71 0.008 MAMC(cm)治疗前21.79±1.26 22.05±1.34 1.03 0.303 1个月后22.48±3.02a 24.18±2.35a 3.25 0.002 TSF(cm)治疗前9.89±2.45 10.33±1.89 1.04 0.301
4.两组患者蛋白水平比较
研究组治疗1个月后ALB、PA、TRF水平均高于对照组(均P<0.05),见表4。
表4 两组慢加急性肝衰竭患者蛋白水平比较()
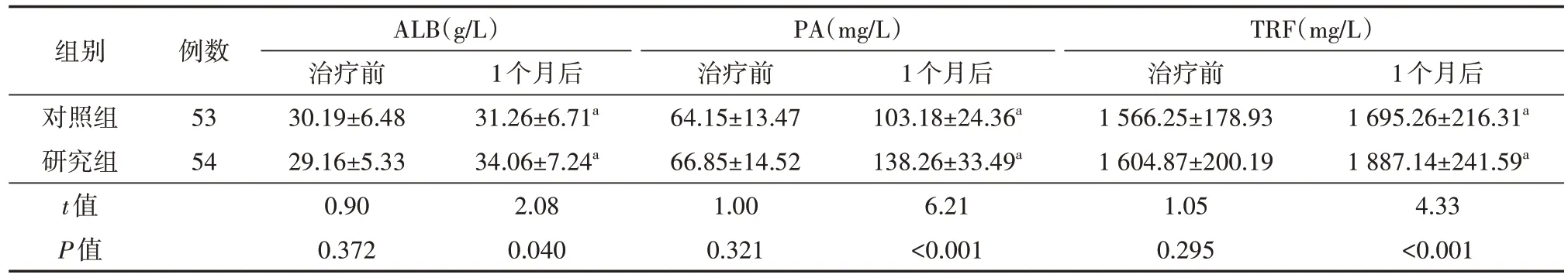
表4 两组慢加急性肝衰竭患者蛋白水平比较()
注:对照组接受日间加餐营养支持治疗,研究组在对照组的基础上增加夜间加餐营养支持治疗;ALB为白蛋白,PA为前白蛋白,TRF为转铁蛋白;与同组治疗前比较,aP<0.05
1个月后1 695.26±216.31a 1 887.14±241.59a 4.33<0.001组别对照组研究组t值P值例数53 54 ALB(g/L)治疗前30.19±6.48 29.16±5.33 0.90 0.372 1个月后31.26±6.71a 34.06±7.24a 2.08 0.040 PA(mg/L)治疗前64.15±13.47 66.85±14.52 1.00 0.321 1个月后103.18±24.36a 138.26±33.49a 6.21<0.001 TRF(mg/L)治疗前1 566.25±178.93 1 604.87±200.19 1.05 0.295
讨论
营养不良不仅会造成机体的防御功能受损和免疫功能降低,还会影响疾病的转归,增加并发症的发生风险与治疗难度,延长住院的时间[17]。相关研究发现,对于存在肝脏疾病的患者给予适当的营养支持可以改善疾病发展过程中出现的代谢物质异常,增强患者的营养状态,避免肝功能的继续恶化[18]。肝衰竭患者的夜间三大营养素氧化率依次为脂肪、蛋白质、碳水化合物,夜间禁食后发生的物质代谢相当于正常人禁食3 d后的情况[19]。谭风雷等[20]报道显示,夜间加餐有助于降低脂肪和蛋白质的氧化分解,增强患者的夜间代谢需求以促进肝功能的稳定恢复。
本研究中,研究组患者治疗1周后的NRS-2002评分较治疗前高,但治疗1个月后的NRS-2002评分低于治疗前,且研究组低于对照组,表明增加夜间加餐营养支持治疗,可以降低患者的营养不良发生风险。NRS-2002评分主要与营养受损状况以及疾病严重程度有关,患者刚入院时多存在因疾病进展出现的食欲不振,同时会接受频繁的空腹检查、腹水检查等,加速患者本身的能量消耗。因此,治疗1周后会出现短暂的营养不良风险增加情况,在持续接受夜间加餐营养支持治疗1个月后,改善了患者夜间禁食期间的营养代谢状况,减缓了肝细胞的衰竭速度,降低了营养不良的发生风险。
本研究中治疗1个月后研究组的Child-Pugh评分低于对照组,表明增加夜间加餐营养支持治疗可以增强患者的肝脏储备功能。正常情况下机体的能量提供以葡萄糖为主,肝衰竭患者因肝功能障碍,导致糖原的合成和储存均减少,夜间保持空腹的时间较长,葡萄糖供能不足便会增加脂肪和蛋白质的分解。因此,肝衰竭患者多存在体质量下降、血清蛋白水平下降的情况,体内蛋白质的不足会导致肝功能难以恢复[21-22]。在患者睡前加餐可以加强夜间的糖氧化过程,减少脂肪和蛋白质的代谢以促进肝细胞的修复,避免营养不良的发生。而血清蛋白水平作为评价营养不良最常用的指标,本研究中研究组的ALB、PA、TRF水平均低于对照组,表明了增加夜间加餐后,患者的营养状态得到了改善。ALB可维持机体营养的稳定,ALB水平升高后可以减少水钠潴留情况的发生,表明机体蛋白质补充足够,机体营养得到改善;PA水平升高后可以避免因疾病问题产生的感染情况,减少了因感染而造成的营养代谢增加;TRF水平升高,表示肝肾功能明显好转[23]。本研究中研究组患者的身体状况得到改善,夜间加餐为患者提供了适当的营养补充,通过合理的计算平衡了营养素的摄入,在减少自身蛋白质和脂肪消耗的同时,避免了对肝脏代谢的负担,有助于促进肝细胞的恢复。相关研究认为,夜间加餐增加了蛋白质的摄入后,可以减少肌肉、骨骼中的氨基酸动员,减少蛋白质的分解,最终改善患者一般身体状况[24]。
综上所述,增加夜间加餐营养支持治疗可以降低经TIPS治疗后的慢加急性肝衰竭患者营养不良发生风险,增强肝脏储备功能,改善患者的身体状况及营养状态。本研究为单中心研究,研究普遍性可能受限,后期需进行多中心的样本研究,进一步验证本研究结论。
作者贡献声明徐晓萌:研究设计、撰写论文;张盼盼:收集资料;宋佳、原翔:数据采集、统计学处理

