以多发骨质破坏为首发表现的急性白血病4例并文献复习
李 哲
贵州省人民医院血液内科,贵州贵阳 550002
急性白血病(acute leukemia,AL)是一种造血系统恶性疾病,分为急性髓系白血病(acute myeloid leukemia,AML)及急性淋巴细胞白血病(acute lymphoblastic leukemia,ALL)两类。临床上,AL以贫血、出血、感染和浸润为特点。进展快,如不治疗,患者常在数周或数月内死亡。但少数患者首发症状不典型,可因某一脏器损害或某一局部症状较为突出而就诊,特别是以骨质破坏、骨痛为突出表现者,易误诊误治为骨关节疾病,因此对于骨破坏起病的患者早期诊断、及时给予针对性的治疗尤为重要。现报道4例以多发骨质破坏为首发表现的AL,分析其临床特点及诊疗经过,并复习相关文献。
1 病例资料
1.1 病例1
女性,63岁,因腰背部疼痛4余月,双下肢疼痛20余d于2018年11月入院。2018年7月无明显诱因出现腰背部疼痛,2018年8月就诊于外院诊断“L1椎体陈旧性压缩骨折”,予行“经皮穿刺球囊扩张椎体成形术”,术后疼痛无明显缓解。2018年9月于外院诊断为“腰椎间盘突出症(L2~5,L5~ S1)”,予“椎间盘射频消融+超氧刀”治疗,症状仍无明显缓解,2018年10月出现双下肢疼痛乏力,外院行胸椎MR 示:T7~8及 T10~ L1椎体变扁:压缩性骨折?其他?胸椎轻度退行性变,为进一步诊治转诊我院。入院后查胸部CT示:双侧多发肋骨、胸骨、胸腰椎多发骨质破坏并胸骨、多发胸腰椎病理性骨折,骨髓瘤?转移瘤?骨盆CT示:骨质疏松,左侧耻骨骨折后改变(图1)。血常规示:白细胞3.65×109/L,血红蛋白45g/L,血小板14×109/L。HBV、HCV、HIV、梅毒、肝肾功能、降钙素、自身抗体谱、甲状腺功能、免疫球蛋白定量、血清蛋白电泳、免疫固定电泳未见异常。骨髓细胞学检查:AL,考虑AML-M1。根据病史及辅助检查结果确诊为AML-M1,患者拒绝化疗,于2019年1月死亡。
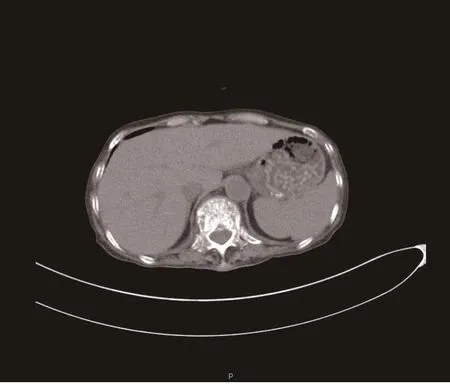
图1 病例1胸部CT
1.2 病例2
男性,40岁,因腰痛伴双下肢疼痛半月于2019年1月入院。2019年1月初无明显诱因出现腰部、双下肢疼痛,就诊当地医院行腰椎MR示:胸11 ~ 12椎体及其附件、腰椎体、骶椎体及其附件、双侧髂骨多发异常信号,考虑骨髓瘤可能性大,不除外转移,转诊我院。入院后查胸腰椎MR示:颈胸腰骶椎及肋骨多发异常信号改变,部分骨质破坏并软组织轻度肿胀,考虑多发性骨髓瘤可能性大(图2)。血常规示:白细胞7.12×109/L,血红蛋白136g/L,血小板283×109/L。HBV、HCV、HIV、梅毒、肝肾功能、免疫球蛋白定量、免疫固定电泳未见异常。行后路经皮腰1椎体病灶穿刺活检术,结果显示:淋巴造血系统肿瘤,结合HE形态及免疫组化标记结果支持为B淋巴母细胞性白血病/淋巴瘤。完善骨髓检查,骨髓细胞学示淋巴高度增生,以畸形原、幼淋为主,占75.5%,提示ALL。免疫分型:异常细胞群体约占有核细胞的88%,主要表达HLA-DR、CD10、CD19、CD22、CD38、cIgM、cCD79a,髓系增殖明显受抑。提示急性B淋巴细胞白血病(前B-ALL可能)。明确诊断为B-ALL。患者拒绝化疗,于2019年5月死亡。
1.3 病例3

图2 病例2胸椎、腰椎MR
男性,48岁,因反复腰痛伴双下肢放射痛、麻木20余日于2019年2月入院。2019年1月无明显诱因出现腰痛、双下肢放射痛伴麻木感,就诊于当地医院予对症治疗后无好转,转诊我院。查胸腰椎MR示:双侧骶骨、髂骨、颈胸腰骶多发椎体及附件多发病灶,部分脊膜增厚,考虑转移瘤可能(图3)。血常规示:白细胞8.16×109/L,血红蛋白110g/L,血小板 101×109/L。HBV、HCV、HIV、梅毒、肝肾功能、免疫球蛋白定量、血清蛋白电泳、免疫固定电泳未见异常。骨髓细胞学:分类见46%白血病细胞,符合AL骨髓象。免疫分型:异常细胞群体约占有核细胞的7.5%,表达HLA-DR、CD10、CD19、CD20、CD38、cIgM、cCD79a。结论:可见异常B淋巴细胞。融合基因无阳性发现。诊断为B-ALL。予VDCLP方案(长春地辛、柔红霉素、环磷酰胺、培门冬酶、地塞米松)化疗,化疗第14天复查骨髓象达完全缓解,化疗结束后血象恢复出院,但未再返院行巩固化疗,于2019年6月死亡。
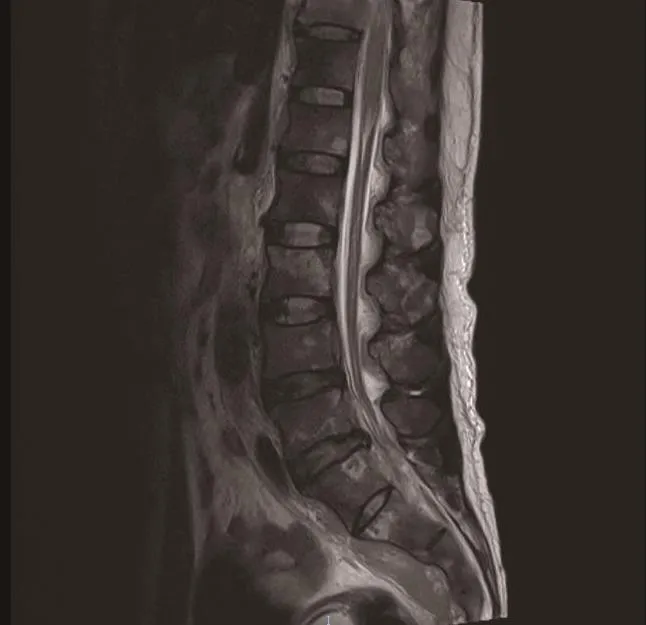
图3 病例3胸椎、腰椎MR
1.4 病例4
女性,21岁,因左小腿疼痛3周于2019年5月入院。2019年5月初无明显诱因感左下肢疼痛,就诊于外院行左膝关节X线片见左胫骨上段骨质破坏,转诊我院。完善相关检查,下肢MR示左侧胫骨上段异常信号,考虑良性病变,非骨化性纤维瘤可能,双侧胫腓骨中上段髓腔信号异常,考虑红黄骨髓转换改变(图4a)。下肢CT示左侧胫骨上段病变,考虑良性病变,非骨化性纤维瘤?骨良性纤维组织细胞瘤?骨纤维异常增殖症?双侧胫腓骨中上段髓腔内密度增高影(图4b)。血常规:白细胞3.11×109/L,血红蛋白 73g/L,血小板 61×109/L,不明细胞23%。HBV、HCV、HIV、梅毒、肝肾功能、降钙素、甲状腺功能、自身抗体谱、免疫球蛋白定量、免疫固定电泳未见异常。骨髓细胞学见单核百分率增高,以原、幼单核细胞增生为主,占85.5%,考虑AML-M5。免疫分型:异常细胞群体约占有核细胞的 61%,主要表达 HLA-DR、CD4、CD7、CD15、CD33、CD38、CD64、CD71、CD117、CD123。提示AML-M5。融合基因无阳性发现。TP53基因突变阳性。染色体核型:47~48,XX,-7,+i(7)(q10),+?i(7)(q10),+8,inc[cp16]/46,XX[4]。 诊 断 为AML-M5。予HAT方案(高三尖杉酯碱、阿糖胞苷、表柔比星)诱导化疗后达完全缓解,流式微小残留病检测阴性,再予HAT方案巩固1疗程、中剂量阿糖胞苷方案巩固1疗程,并予腰椎穿刺、鞘内注射治疗2次,脑脊液检查未见异常。治疗期间监测骨髓细胞学持续完全缓解,流式微小残留病持续阴性。3疗程化疗结束后自行停止化疗,亦未返院复查,至2020年4月仍存活。
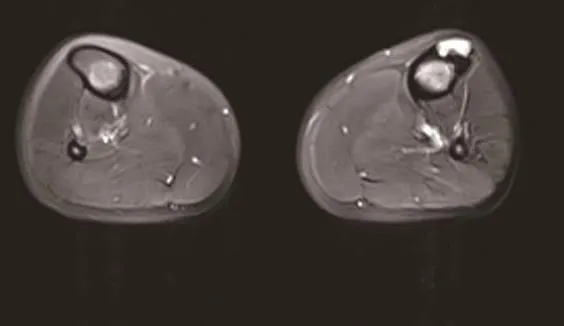
图4 a 病例4下肢MR
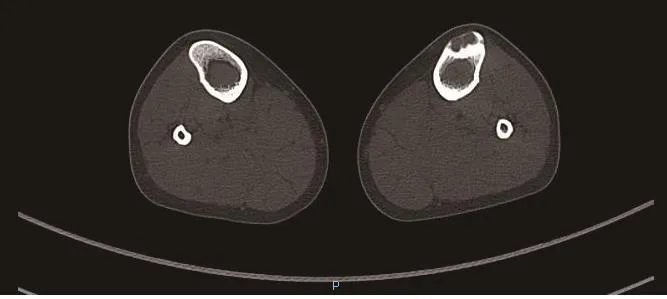
图4 b 病例4下肢CT
2 讨论
AL多数起病急骤,表现为贫血、出血、 感染和浸润等相关症状,但其临床异质性大,并不一定每例患者均出现上述症状。上述病例的共同特点是以骨破坏、骨痛症状起病,仅1例患者(病例1)有乏力症状,4例患者均无出血、发热等白血病典型表现。AL患者外周血象通常表现为白细胞升高、贫血及血小板减少,但上述患者中2例(病例2、3)血常规大致正常,2例患者(病例1、4)可见贫血、血小板减少,全部患者白细胞均未见升高,与AL典型血液学改变不符,如未行骨髓检查极易导致疾病漏诊、误诊。特别是病例1,先后误诊为椎体骨折、椎间盘突出等疾病,并行手术治疗,起病4余月后才得以确诊,既增加了患者痛苦,又延误了白血病的诊治。通过文献回顾,检索出以骨破坏为首发表现的AL的报道比较少见,其中儿童较成人多见,成人骨破坏起病的AL患者中ALL较AML更为常见。
2003 年Haytac等[1]报道了一例14岁ALL男患,以牙槽骨的进行性溶骨性病变为首发表现,血象示贫血、白细胞仅轻度升高。2004年Chang等[2]报道了一例 ALL患者治疗后缓解期出现突眼表现,影像学检查提示眶周溶骨性改变,复查骨髓提示ALL复发。2011年Chung等[3]报道一例35岁男患,以下颌骨破坏起病,血常规仅见轻度贫血,白细胞计数、分类及血小板计数均正常,经骨髓检查诊断为ALL。2014年Verma等[4]报道一例27岁女患因胸背部疼痛起病,病程中出现瘫痪,颅骨平片见多发骨破坏,脊髓MR可见脊髓受压,一度误诊为多发性骨髓瘤,进一步完善骨髓检查确诊为ALL。2015年Kaiafa等[5]报道一例缓解期的B-ALL患者,因腰痛就诊,影像学见腰椎、骶骨、髂骨多发骨质破坏,骨髓检查证实白血病复发。2017年Nikki等[6]报道一例24岁男患,以背痛起病,脊椎及肋骨可见多发骨破坏,骨髓检查证实ALL。2009年,我国学者徐燕等[7]报道一例17岁男性,以多发骨痛起病,颅骨、骨盆、胸腰椎、肋骨多发骨质破坏,骨髓象诊断为ALL。2014年张丽等[8]报道一例以腰痛为首发表现的56岁男患,初诊为“椎间盘突出”,行物理治疗及中药治疗,腰痛无缓解并出现肋骨疼痛。行胸腰椎MR提示:胸腰段多个椎体及双侧髂骨内见片团状混杂信号影,部分椎体压缩变扁、病理性骨折,通过骨髓细胞学等检查确诊为ALL。2018年文小亮等[9]报道一例45岁女患,主诉髋部、骶尾部疼痛不适,MR示胸椎、腰骶椎、双侧髂骨、骶骨多发异常信号影,进一步行骨髓穿刺明确诊断ALL。2019年马婕等[10]报道一例以多发骨质破坏为首发表现的ALL患者,主因骨盆部、腰背部疼痛就诊,行MR示腰椎、髂骨、骶骨、髋臼、耻骨、坐骨及股骨异常信号影,考虑“骨肿瘤,骨转移瘤”可能,血常规未见异常,行骨髓检查后得以诊断。
相对于ALL,AML并发的骨质破坏更为罕见。2000年Lima等[11]报道一例17岁男性患者,以腰痛起病,CT及骨扫描示溶骨性改变,完善骨髓检查诊断为AML。诱导化疗后复查骨髓细胞学和骨髓活检未见白血病细胞,但骨扫描异常病灶持续存在,12月后白血病复发。2012年Tucker等[12]报道一例53岁男患,既往诊断骨髓增生异常综合征,以骨痛起病,影像学检查发现多发溶骨性病变,复查骨髓细胞学提示已进展为AML。2016年Chambers等[13]报道一例62岁女患,既往诊断真性红细胞增多症,以晕厥起病,影像学检查示胸椎及颅骨多发溶骨性改变,完善骨髓细胞学、免疫分型、CD45染色等检查后诊断为AML。2001年我国学者董家蔷等[14]报道一例 56岁男性,以骨痛起病,初诊时诊断为股骨头坏死,但对治疗反应差,1月后行骨扫描检查显示全身多发骨质破坏,行骨髓涂片、免疫分型等检查明确诊断为AML-M2。2013年黄乐等[15]报道了一例21岁男患,以多发骨痛起病,胸椎及右侧4、5肋多发骨破坏,颅骨多发斑点状、斑片状骨质破坏区,同时伴有肾功能损害,完善骨髓穿刺检查除外多发性骨髓瘤,诊断为AML-M2。
急性白血病是具有增殖及生存优势的原始、幼稚细胞在造血组织中异常增生,并侵袭至其他组织器官,使正常造血受到抑制。生长中的骨骼是白血病细胞重要的增殖场所。成年人骨髓腔中脂肪组织较多,且间隙大,白血病细胞增生时只取代脂肪组织,而骨浸润破坏少见。ALL导致骨破坏的机制尚有争议,多数研究认为与促炎细胞因子有关。Fukasawa等[16]在一例多发骨破坏并高钙血症的B-ALL患者血清中检出高浓度的肿瘤坏死因子α (tumor necrosis factor-alpha,TNF-α)、白细胞介素(interleukin,IL)-6、可溶性 IL-2受体,诱导化疗后血钙降至正常,TNF-α、IL-6、可溶性IL-2受体水平均下降,提示高水平的促炎细胞因子可能在ALL骨损害中发挥作用。Niizuma等[17]研究认为ALL患者中高水平的TNF-α、IL-6可刺激破骨细胞性骨吸收,从而参与骨破坏。Virijevic等[18]发现ALL患者TNF-α水平升高,IL-1α、IL-1β水平正常,考虑TNF-α是ALL骨损害的致病因素。而Poirée等[19]认为ALL患者血清甲状旁腺激素相关肽(PTHrP)水平升高,PTHrP可能与多处溶骨性病变和高钙血症有关。应注意的是,上述研究均为个案研究,因此结论的可靠性尚待进一步验证。AML引起骨损害的机制亦无定论,在目前有限的研究中,Fisch等[20]发现白血病小鼠血清中骨形成标志物骨钙素水平降低,成骨细胞和骨内膜内骨桥蛋白细胞减少,导致严重的矿化骨丢失。在模型小鼠和AML患者中趋化因子ccl-3 mRNA表达上调,而ccl-3已在骨髓瘤中被证实可抑制成骨细胞的功能,考虑ccl-3参与了AML骨破坏的发生。
以骨质破坏为首发临床表现的急性白血病,其骨质破坏往往出现在血液学改变之前,且多以骨痛为首发症状,若不仔细甄别,容易导致疾病的误诊、漏诊而延误治疗。因此在患者以骨痛、多发性骨破坏就医时,除考虑到原发于骨骼的病变外,还应考虑到急性白血病,及时完善骨髓细胞学、免疫分型、染色体、融合基因等相关检查,以尽快明确诊断、及时治疗。

