双溴代马蹄金素衍生物的合成及其抗HBV活性
梁光平,胡占兴,黄正明,刘青川,张建新,梁光义,徐必学
(1.贵州省中国科学院天然产物化学重点实验室,贵州 贵阳 550002;2.贵阳中医学院 药学院,贵州 贵阳 550002;3.中国人民解放军第302医院 药学部,北京 丰台 100039)
乙肝是由乙肝病毒(Hepatitis B virus, HBV)感染引起的,全球估计有20亿人感染乙肝病毒,约有4亿人患有慢性肝脏感染疾病,绝大部分人群分布在亚太地区[1]。全球每年有上百万人死于乙肝病毒感染的相关疾病[2-3],以拉米夫定为代表的核苷类药物和以干扰素-α为代表的生物类免疫调节剂等主流药物均存在不良反应、耐药以及价格昂贵等缺陷。因此,寻找和开发新的抗乙肝病毒药物具有重要的意义[4]。
马蹄金素[N-(N-苯甲酰基-L-苯丙氨酰基)-O-乙酰基-L-苯丙氨醇,MTS]是本研究组从马蹄金(DichondrarepensForst.)中分离到的化合物,具有较好的抗HBV活性(见图1),查阅资料发现该化合物是新化学骨架类型的抗乙肝病毒化合物。对其进行结构修饰得到一系列衍生物,体外抗HBV活性测试发现其中有一些化合物具有较好的抗乙肝病毒活性[5-8]。而含溴的化合物在抗病毒方面具有良好的抑制活性[9-10],本文以马蹄金素为先导化合物,设计合成具有双溴取代的马蹄金素类似物,并对其进行初步的体外抗HBV活性测试,以期在拓宽马蹄金素结构修饰产物类型的同时,获得更多具有深入研究价值的修饰产物。
1 仪器与试剂
核磁共振谱以TMS为内标,用Inova-400 MHz型超导核磁共振仪(美国Varian公司)测定。质谱用HP-5793质谱仪测定(美国Hewlett-Packard公司)。柱色谱用硅胶(300~400目)为青岛海洋化工厂产品。其余试剂均为市售分析纯或化学纯产品,除特别说明外,未经处理直接使用。6,8-二溴-L-酪氨酸(化学纯,BDH试剂)、L-苯丙氨醇(纯度99%,扬州宝盛生物化工有限公司)和L-苯丙氨酸甲酯(纯度99%,扬州宝盛生物化工有限公司)。
2 实验内容
2.1 目标化合物的合成路线 合成路线如图2所示,以6,8-二溴-L-酪氨酸为起始原料,在SOCl2以及CH3OH的作用下得化合物1;化合物1与苯甲酸在氯甲酸异丁酯(IBCF)和N-甲基吗啉(NMM)的作用下反应得到化合物2,再经碱水解得化合物3,在IBCF-NMM存在下,化合物3与L-苯丙氨醇缩合得化合物4,化合物3与L-苯丙氨酸甲酯盐酸盐反应得化合物6,化合物4经取代反应得化合物5a~5e,化合物6经取代反应后得化合物7a~7d。
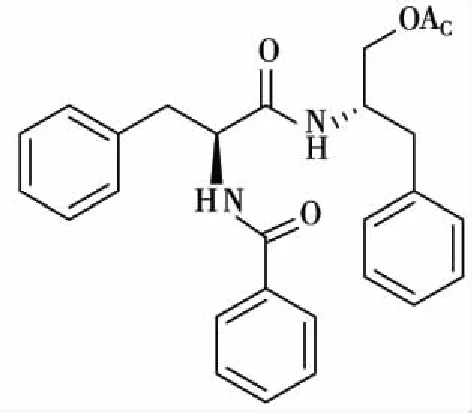
图1 马蹄金素的化学结构
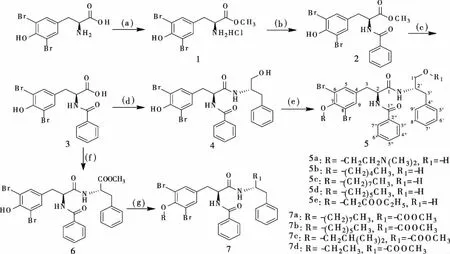
图2 目标化合物的合成路线
试剂及反应条件: (a) MeOH, SOCl2, rt, 2.5 h, then reflux for 30 min; (b) benzoic acid, IBCF, NMM, CH2Cl2, DMF, -5oC to rt, 8 h; (c) NaOH, DMF, rt, 1 h; (d) L-phenylalanol, IBCF, NMM, CH2Cl2, DMF, -5oC to rt, 8 h; (e) 1-Iodooctane or 1-bromohexane or 1-iodo-2-methylpropane or iodoethane, 1,4-dioxane, K2CO3, rt; (f) L-phenylalanine methyl ester hydrochloride, CH2Cl2, DMF, IBCF, NMM, -5oC to rt, 8 h; (g) 2-Dimethylaminoethyl chloride hydrochloride or 1-bromopentane or 1-iodooctane or 1-bromohexane or ethyl chloroacetate, DMF, K2CO3, rt。
2.2 化学合成 6,8-二溴-L-酪氨酸甲酯盐酸盐①N-苯甲酰基-6,8-二溴-L-酪氨酸甲酯②和N-苯甲酰基-6,8-二溴-L-酪氨酸③的合成根据参考文献[5]的方法即可合成,3步反应总收率为60%左右。
N-(N-苯甲酰基-6,8-二溴-L-酪氨酰基)-L-苯丙氨醇(4)的合成:取化合物3(6.65 g,15.0 mmol),L-苯丙氨醇(2.72 g,18.0 mmol)于反应瓶中,65℃真空干燥1 h后,在氩气保护下,加入经分子筛干燥的DMF(50 mL)和CH2Cl2(100 mL)溶解完全,加入NMM(3.9 mL,34.5 mmol),冰盐浴冷却下,缓慢滴加含IBCF(2.4 mL,18.0 mmol)的CH2Cl2溶液20 mL。滴毕,继续搅拌,TLC跟踪反应,约8 h反应完全,加少量水终止反应,减压回收CH2Cl2,用乙酸乙酯(500 mL×2)萃取,有机层依次以水、稀盐酸、饱和NaHCO3溶液洗涤,无水MgSO4干燥,减压回收乙酸乙酯至有大量固体析出,冷却过滤,滤饼干燥即得化合物4(7.2 g,产率83%)。m.p. 234~236℃;ESI-MSm/z: 577.1 [M+H]+;1H-NMR (DMSO-d6) δ: 9.22 (s, 1H, 7-OH), 8.54 (d,J= 7.6 Hz, 1H, 1′′-CONH), 8.47 (d,J= 8.8 Hz, 1H, 1-CONH), 7.75 (d,J= 7.0 Hz, 2H, H-3′′, 7′′), 7.51 (m, 3H, H-4′′-6′′), 7.44 (m, 2H, H-6′, 8′), 7.26-7.17 (m, 5H, H-5, 9, 5′, 7′, 9′), 4.84 (t,J= 5.2 Hz, 1H, 1′-OH), 4.65 (m, 1H, H-2), 4.49 (m, 1H, H-2′), 3.20 (m, 2H, H-3), 2.95 (m, 2H, H-3′);13C-NMR (DMSO-d6) δ: 171.9, 171.4, 166.5, 149.1, 137.0, 134.0, 133.0, 132.9, 131.5, 129.2, 128.4, 128.3, 127.4, 126.7, 111.6, 62.2, 54.5, 53.8, 36.7, 35.5. Anal. calcd for C25H24Br2N2O4:C 52.10, H 4.20, N 4.86; found C 52.09, H 4.21, N 4.84。
N-(N-苯甲酰基-O-二甲氨基乙基-6,8-二溴-L-酪氨酰基)-L-苯丙氨醇(5a)的合成:取化合物4(200 mg,0.35 mmol)、无水K2CO3(290 mg,2.1 mmol)和二甲氨基氯乙烷盐酸盐(60 mg,21.08 mmol)置于反应瓶中,加入1,4-二氧六环70 mL,再加入碳酸钾质量10%的水,100~105℃油浴中回流3.5 h使之反应完毕(TLC检测)。反应液冷却至室温,加入乙酸乙酯(200 mL)和水(100 mL)萃取,乙酸乙酯层用0.1 mol/L盐酸反萃取,取酸水层,以0.2 mol/L的NaOH水溶液调pH 8~9,加入乙酸乙酯(200 mL)萃取,有机层经水洗一次,无水MgSO4干燥,回收溶剂至干,残留物经硅胶柱层析(氯仿︰甲醇,25︰1)得化合物5a(162 mg,收率为72%)。m.p. 218~221°C; ESI-MSm/z: 648.2 [M+H]+;1H-NMR (DMSO-d6) δ: 8.51 (d,J= 8.8 Hz, 1H, 1′′-CONH), 7.94 (d,J= 8.4 Hz, 1H, 1-CONH), 7.80 (d,J= 7.2 Hz, 2H, H-3′′, 7′′), 7.64 (s, 2H, H-5, 9), 7.55-7.44 (m, 3H, H-6′-8′), 7.24-7.12 (m, 5H, H-4′′-6′′, 5′, 9′), 4.83 (m, 1H, H-2), 4.70-4.63 (m, 1H, H-2′), 3.95 (t,J= 6.0 Hz, 1H, -OH), 3.90 (m, 2H, 7-OCH2CH2N), 3.37-3.31 (m, 4H, H-3, 1′), 3.01 (m, 1H, H-3′a), 2.94-2.85 (m, 2H, 7-OCH2CH2N), 2.70-2.65 (m, 1H, H-3′b), 2.21 (s, 6H, -N(CH3)2);13C-NMR (DMSO-d6) δ: 170.4, 166.3, 150.9, 138.9, 137.8, 134.0, 133.5, 131.3, 129.1, 128.2, 128.0, 127.3, 125.9, 117.0, 71.2, 62.1, 58.1, 54.5, 52.5, 45.4, 36.4, 35.9. Anal. calcd for C29H33Br2N3O4: C 53.80, H 5.14, N 6.49; found C 53.47, H 5.28, N 6.52。
N-(N-苯甲酰基-O-正戊基-6,8-二溴-L-酪氨酰基)-L-苯丙氨醇(5b)的合成:取化合物4 (150 mg, 0.26 mmol)和无水K2CO3(290 mg, 0.21 mmol)置于反应瓶中, 依次加入DMF(10 mL),溴代正戊烷(1.30 mmol),所得混合物于50 ℃油浴中搅拌4.5 h至反应完毕(TLC检测)。待反应液冷却至室温后, 加入乙酸乙酯(200 mL)和水(100 mL)萃取,有机层经水洗,无水MgSO4干燥,浓缩,残留物经硅胶柱层析(石油醚∶乙酸乙酯,4∶1)得85 mg白色固体5b,产率为50%。m.p. 207~210 °C; ESI-MSm/z: 669.4 [M+Na]+;1H-NMR (CDCl3) δ: 8.50 (d,J=8.4 Hz, 1H, 1′′-CONH), 7.97 (d,J= 8.4 Hz, 1H, 1-CONH), 7.80 (d,J= 7.2 Hz, 2H, H-3′′, 7′′), 7.64 (s, 2H, H-5, 9), 7.54 (m, 1H, H-7′), 7.46 (m, 2H, H-6′, 8′), 7.24-7.14 (m, 5H, H-4′′-6′′, 5′, 9′), 4.84 (m, 1H, H-2), 4.66 (m, 1H, H-2′), 3.89 (m, 3H, 1′-OH, 7-OCH2(CH2)3CH3), 3.32 (m, 2H, H-1′), 3.04-2.87 (m, 3H, H-3, 3′a), 2.66 (m, 1H, H-3′b), 1.76 (m, 2H, 7-OCH2CH2(CH2)2CH3), 1.46(m, 2H, 7-O(CH2)2CH2CH2CH3), 1.28 (m, 2H, 7-O(CH2)3CH2CH3), 0.91 (t,J= 7.0 Hz, 3H, 7-O(CH2)5CH3);13C-NMR (CDCl3) δ: 170.4, 166.2, 150.9, 139.0, 137.8, 134.0, 133.4, 131.3, 129.0, 128.2, 128.0, 127.3, 125.9, 117.0, 67.3, 62.1, 54.5, 52.5, 36.4, 35.9, 29.4, 25.7, 22.0, 14.0. Anal. calcd for C30H34Br2N2O4: C 55.74, H 5.30, N 4.33; found C 55.75, H 5.27, N 4.34。
N-(N-苯甲酰基-O-正辛基-6,8-二溴-L-酪氨酰基)-L-苯丙氨醇(5c)的合成:取化合物4(100 mg)、无水碳酸钾(192 mg,1.4 mmol)、碘代正辛烷(210 mg, 0.9 mmol),参照化合物5b的制备方法得到72 mg白色粉末,收率为60%。m.p. 233~235 °C; ESI-MSm/z: 689.4 [M+H]+;1H-NMR (CDCl3) δ: 8.53 (d,J= 8.4 Hz, 1H, 1′′-CONH), 7.97 (d,J= 8.0 Hz, 1H, 1-CONH), 7.80 (d,J= 7.2 Hz, 2H, H-3′′, 7′′), 7.65 (s, 2H, H-5, 9), 7.53 (m, 1H, H-7′), 7.46 (m, 2H, H-6′, 8′), 7.24-7.18 (m, 4H, H-4′′, 6′′, 5′, 9′), 7.14 (m, 1H, H-5′′), 4.84 (t,J= 5.2 Hz, 1H, 1′-OH), 4.65 (m, 1H, H-2), 3.91 (m, 1H, H-2′), 3.87 (d,J= 6.4 Hz, 2H, 7-OCH2(CH3)6CH3), 3.35-3.28 (m, 2H, H-1′), 3.03-2.85 (m, 3H, H-3, 3′a), 2.67 (m, 1H, H-3′b), 1.72 (m, 2H, 7-OCH2CH2(CH2)5CH3), 1.44 (m, 2H, 7-O(CH2)2CH2(CH2)4CH3), 1.26 (m, 8H, 7-O(CH2)3(CH2)4CH3), 0.85 (t,J= 6.8 Hz, 3H, 7-O(CH2)7CH3);13C-NMR (CDCl3) δ: 170.4, 166.3, 150.9, 138.8, 137.7, 134.0, 133.5, 131.3, 129.1, 128.1, 128.0, 127.3, 125.8, 117.0, 73.0, 62.1, 54.4, 52.5, 36.4, 35.9, 31.2, 29.4, 28.7, 28.5, 25.3, 22.0, 13.9. Anal. calcd for C33H40Br2N2O4: C 57.57, H 5.86, N 4.07; found C 57.55, H 5.85, N 4.10。
N-(N-苯甲酰基-O-正己基-6,8-二溴-L-酪氨酰基)-L-苯丙氨醇(5d)的合成:取化合物4(100 mg)、无水碳酸钾(192 mg, 1.4 mmol)、溴代正己烷(143 mg, 0.9 mmol),参照化合物5b的制备方法得到75 mg白色粉末,收率为65%。m.p. 229~232 °C; ESI-MSm/z: 661.4 [M+H]+;1H-NMR (CDCl3) δ: 8.52 (d,J= 8.8 Hz, 1H, 1′′-CONH), 7.96 (d,J= 8.4 Hz, 1H, 1-CONH), 7.80 (d,J= 7.2 Hz, 2H, H-3′′, 7′′), 7.64 (s, 2H, H-5, 9), 7.54 (m, 1H, H-7′), 7.46 (m, 2H, H-6′, 8′), 7.24-7.14 (m, 5H, H-4′′-6′′, 5′, 9′), 4.84 (m, 1H, H-2), 4.66 (m, 1H, H-2′), 3.91-3.85 (m, 3H, 1′-OH, 7-OCH2(CH2)4CH3), 3.37-3.28 (m, 2H, H-1′), 3.02-2.85 (m, 3H, H-3, 3′a), 2.66 (m, 1H, H-3′b), 1.74 (m, 2H, 7-OCH2CH2(CH2)3CH3), 1.44 (m, 2H, 7-O(CH2)2CH2(CH2)2CH3), 1.29 (m, 4H, 7-O(CH2)3(CH2)2CH3), 0.87 (t,J= 6.8 Hz, 3H, 7-O(CH2)5CH3);13C-NMR (CDCl3) δ: 170.4, 166.3, 150.9, 138.9, 137.8, 134.0, 133.5, 131.3, 129.1, 128.2, 128.0, 127.3, 125.9, 117.0, 73.0, 62.1, 54.5, 52.5, 36.4, 35.9, 31.0, 29.4, 24.9, 22.0, 13.9. Anal. calcd for C31H36Br2N2O4: C 56.38, H 5.49, N 4.24; found C 56.09, H 5.84, N 4.64。
N-(N-苯甲酰基-O-乙酸乙酯基-6,8-二溴-L-酪氨酰基)-L-苯丙氨醇(5e)的合成:取化合物4(100 mg)、无水碳酸钾(192 mg, 1.4 mmol)、氯乙酸乙酯(106 mg, 0.9 mmol),参照化合物5b的制备方法得到47 mg白色粉末,收率为41%。m.p. 155~157°C; ESI-MSm/z: 663.2 [M+H]+;1H-NMR (CDCl3) δ: 8.53 (d,J= 8.4 Hz, 1H, 1′′-CONH), 7.96 (d,J= 8.4 Hz, 1H, 1-CONH), 7.81 (d,J= 7.2 Hz, 2H, H-3′′, 7′′), 7.64 (s, 2H, H-5, 9), 7.54 (m, 1H, H-7′), 7.46 (m, 2H, H-6′, 8′), 7.24-7.14 (m, 5H, H-4′′-6′′, 5′, 9′), 4.86 (t,J= 5.0 Hz, 1H, 1′-OH), 4.68 (m, 2H, H-2, 2′), 4.42 (s, 2H, 7-OCH2COOCH2CH3), 3.94 (m, 2H, 7-OCH2COOCH2CH3), 3.32 (m, 2H, H-1′), 3.04-2.87 (m, 3H, H-3, 3′a), 2.66 (m, 1H, H-3′b), 1.28 (t,J= 6.8 Hz, 3H, 7-OCH2COOCH2CH3);13C-NMR (CDCl3) δ: 171.4, 170.2, 166.1, 150.9, 139.0, 137.9, 134.1, 133.4, 131.3, 129.0, 128.2, 128.0, 127.3, 125.7, 118.3, 70.1, 66.9, 62.5, 54.9, 52.5, 36.9, 35.9, 14.1. Anal. calcd for C29H30Br2N2O6: C 52.59, H 4.57, N 4.23; found C 52.25, H 4.54, N 4.04。
N-(N-苯甲酰基-6,8-二溴-L-酪氨酰基)-L-苯丙氨酸甲酯(6)的合成:取化合物3(4.43 g,10.0 mmol),L-苯丙氨酸甲酯盐酸盐(2.59 g,12.0 mmol),NMM(2.6 mL,23.0 mmol),IBCF(1.6 mL,12.0 mmol),按化合物4的合成方法进行,得化合物6(4.9 g,产率81.1%)。m.p. 218~219°C; ESI-MSm/z: 627.0 [M+Na]+;1H-NMR (DMSO-d6, 400 MHz) δ: 8.55 (d,J= 7.6 Hz, 1H, 1′′-CONH), 8.47 (d,J= 8.8 Hz, 1H, 1-CONH), 7.75 (d,J= 6.8 Hz, 2H, H-3′′, 7′′), 7.51 (m, 3H, H-4′′-6′′), 7.44 (m, 2H, H-6′, 8′), 7.26-7.17 (m, 5H, H-5, 9, 5′, 7′, 9′), 4.65 (m, 1H, H-2), 4.49 (m, 1H, H-2′), 3.58 (s, 3H, 1′-OCH3), 3.20 (m, 2H, H-3), 2.95 (m, 2H, H-3′);13C-NMR (DMSO-d6) δ: 171.9, 171.4, 166.5, 149.1, 137.0, 134.0, 133.0, 132.9, 131.5, 129.2, 128.4, 128.3, 127.4, 126.7, 111.6, 54.5, 53.8, 52.0, 36.7, 35.5. Anal. calcd for C26H24Br2N2O5: C 51.68, H 4.00, N 4.64; found C 51.65, H 4.01, N 4.63。
N-(N-苯甲酰基-O-正辛基-6,8-二溴-L-酪氨酰基)-L-苯丙氨酸甲酯(7a)的合成:取化合物6(100 mg)、无水碳酸钾(183 mg, 1.3 mmol)、碘代正辛烷(200 mg, 1.3 mmol),参照化合物7a的制备方法得到79 mg白色粉末,收率为67%。m.p. 177~179°C; ESI-MSm/z: 739.2 [M+Na]+;1H-NMR (DMSO-d6) δ: 8.55-8.51 (m, 2H, 1-CONH, 1′′-CONH), 7.76-7.74 (m, 2H, H-3′′, 7′′), 7.64 (s, 2H, H-5, 9), 7.53-7.49 (m, 1H, H-7′), 7.45-7.41 (m, 2H, H-6′, 8′), 7.26-7.16 (m, 5H, H-4′′-6′′, 5′, 9′), 4.73-4.67 (m, 1H, H-2), 4.54-4.48 (m, 1H, H-2′), 3.84 (m, 2H, 7-OCH2(CH2)6CH3), 3.58 (s, 3H, 1′-OCH3), 3.07-2.84 (m, 4H, H-3, 3′), 1.74-1.67 (m, 2H, 7-OCH2CH2(CH2)6CH3), 1.45-1.37 (m, 2H, 7-O(CH2)2CH2(CH2)4CH3), 1.26-1.22 (m, 8H, 7-O(CH2)3(CH2)4CH3), 0.87-0.81 (m, 3H, 7-OCH2(CH2)6CH3);13C-NMR (DMSO-d6) δ: 171.9, 171.3, 166.6, 151.1, 137.7, 137.0, 134.0, 133.6, 131.5, 129.2, 128.4, 128.3, 127.5, 126.7, 117.2, 73.1, 54.3, 53.8, 52.0, 36.8, 35.7, 31.3, 29.5, 28.8, 28.7, 25.4, 22.2, 14.1. Anal. calcd for C34H40Br2N2O5: C 56.99, H 5.63, N 3.91; found C 57.45, H 5.65, N 4.03。
N-(N-苯甲酰基-O-正己基-6,8-二溴-L-酪氨酰基)-L-苯丙氨酸甲酯(7b)的合成:取化合物6(100 mg)、无水碳酸钾(183 mg, 1.3 mmol)、溴代正己烷(137 mg, 0.8 mmol),参照化合物7b的制备方法得到62 mg白色粉末,收率为54%。m.p. 149~151°C; ESI-MSm/z: 711.2 [M+Na]+;1H-NMR (DMSO-d6) δ:8.55 (m, 2H, 1-CONH, 1′′-CONH), 7.75 (m, 2H, H-3′′, 7′′), 7.64 (s, 2H, H-5, 9), 7.53-7.49 (m, 1H, H-7′), 7.43 (m, 2H, H-6′, 8′), 7.26-7.16 (m, 5H, H-4′′-6′′, 5′, 9′), 4.74-4.68 (m, 1H, H-2), 4.54-4.49 (m, 1H, H-2′), 3.84 (t,J= 6.4 Hz, 2H, 7-OCH2(CH2)4CH3), 3.58 (s, 3H, 1′-OCH3), 3.07-2.84 (m, 4H, H-3, 3′), 1.74-1.67 (m, 2H, 7-OCH2CH2(CH2)3CH3), 1.45-1.38 (m, 2H, 7-O(CH2)2CH2(CH2)2CH3), 1.30-1.25 (m, 4H, 7-O(CH2)3(CH2)2CH3), 0.85 (t,J= 7.2 Hz, 3H, 7-O(CH2)5CH3);13C-NMR (DMSO-d6) δ: 171.8, 171.3, 166.6, 151.1, 137.7, 136.9, 134.0, 133.6, 131.5, 129.2, 128.4, 128.3, 127.4, 126.7, 117.2, 73.2, 54.3, 53.8, 52.0, 36.8, 35.7, 31.1, 29.5, 25.1, 22.1, 14.0. Anal. calcd for C32H36Br2N2O5: C 55.21, H 5.08, N 4.15; found C 55.89, H 5.650, N 4.23。
N-(N-苯甲酰基-O-异丁基-6,8-二溴-L-酪氨酰基)-L-苯丙氨酸甲酯(7c)的合成:取化合物6(100 mg)、无水碳酸钾(183 mg, 1.3 mmol)、碘代异丁烷(152 mg, 0.83 mmol),参照化合物7c的制备方法得到44 mg白色粉末,收率为40%。m.p. 211-213°C; ESI-MSm/z: 683.2 [M+Na]+;1H-NMR (DMSO-d6) δ: 8.57-8.53 (m, 2H, 1-CONH, 1′′-CONH), 7.77-7.74 (m, 2H, H-3′′, 7′′), 7.65 (s, 2H, H-5, 9), 7.53-7.49 (m, 1H, H-7′), 7.45-7.41 (m, 2H, H-6′, 8′), 7.26-7.16 (m, 5H, H-4′′-6′′, 5′, 9′), 4.73-4.68 (m, 1H, H-2), 5.54-4.48 (m, 1H, H-2′), 3.65 (d,J= 8.4 Hz, 2H, 7-OCH2CH(CH3)2), 3.58 (s, 3H, 1′-OCH3), 3.07-2.84 (m, 4H, H-3, 3′), 2.08-2.00 (m, 1H, 7-OCH2CH(CH3)2), 0.98 (d,J= 6.8 Hz, 6H, 7-OCH2CH(CH3)2);13C-NMR (DMSO-d6) δ: 171.8, 171.2, 166.6, 150.9, 137.6, 136.9, 134.0, 133.6, 131.5, 129.1, 128.3, 127.4, 126.7, 117.1, 78.9, 54.2, 53.8, 52.0, 36.7, 35.6, 28.7, 19.1. Anal. calcd for C30H32Br2N2O5: C 54.56, H 4.88, N 4.24; found C 54.37, H 5.19, N 4.47。
N-(N-苯甲酰基-O-乙基-6,8-二溴-L-酪氨酰基)-L-苯丙氨酸甲酯(7d)的合成:取化合物6(100 mg)、无水碳酸钾(183 mg, 1.3 mmol)、碘代正辛烷(129 mg, 0.83 mmol),参照化合物7d的制备方法得到29 mg白色粉末,收率为28%。m.p. 185~188°C; ESI-MSm/z: 655.2 [M+Na]+;1H-NMR (DMSO-d6) δ: 8.54 (m, 2H, 1′′-CONH, 1-CONH), 7.76 (m, 2H, H-3′′, 7′′), 7.65 (s, 2H, H-5, 9), 7.50 (t,J= 7.6 Hz, 1H, H-7′), 7.44 (m, 2H, H-6′, 8′), 7.24-7.19 (m, 5H, H-4′′-6′′, 5′, 9′), 4.71 (m, 1H, H-2), 4.52 (m, 1H, H-2′), 3.93 (m, 2H, 7-OCH2CH3), 3.34 (s, 3H, 1′-COOCH3), 3.04-2.99 (m, 3H, H-3, 3′a), 2.89 (dd,J1= 2.0,J2= 11.2 Hz, 1H, H-3′b), 1.33 (t,J= 7.0 Hz, 3H, 7-OCH2CH3);13C-NMR (DMSO-d6) δ: 171.7, 171.1, 166.4, 151.0, 137.6, 136.9, 133.9, 133.5, 131.4, 129.1, 128.3, 128.2, 127.3, 126.6, 117.1, 69.1, 54.1, 53.7, 51.9, 36.7, 35.6, 15.3. Anal. calcd for C28H28Br2N2O5:C 53.18, H 4.46, N 4.43; found C 52.98, H 4.51, N,4.47。
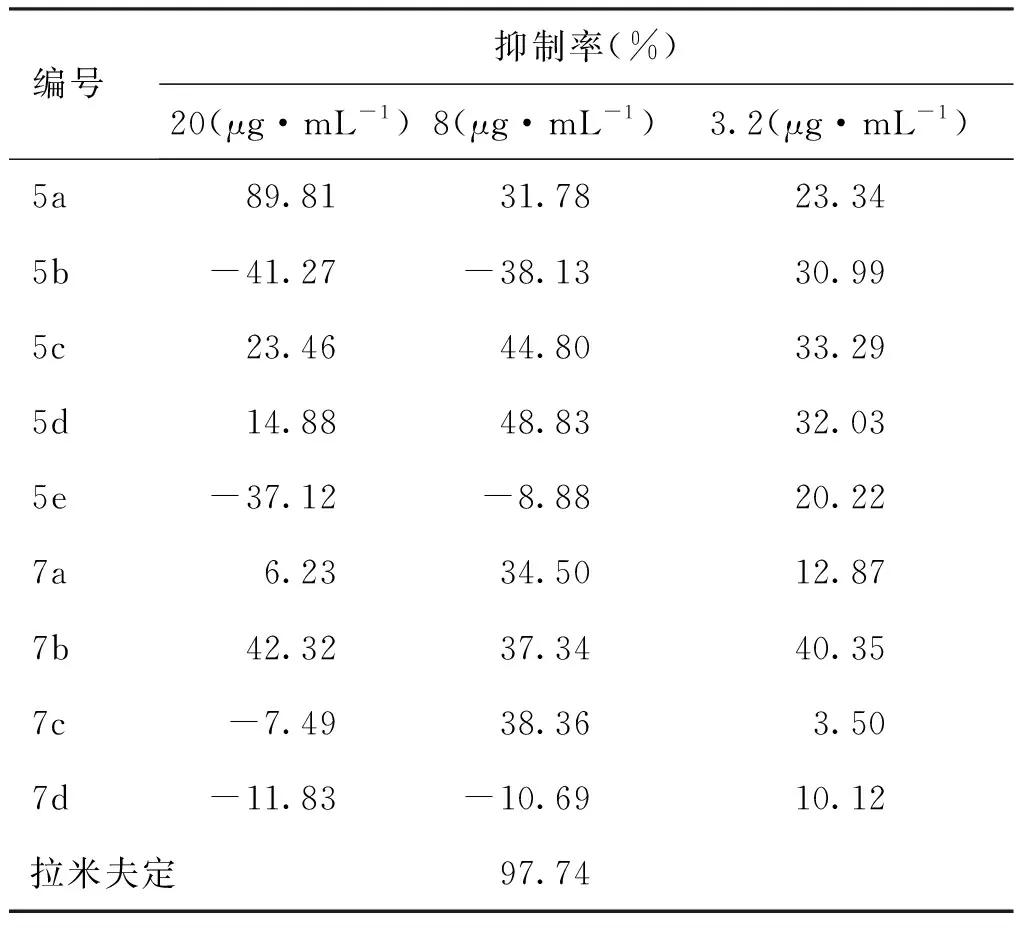
2.3 体外抗HBV活性筛选 HepG22.2.15细胞每毫升20万个接种24孔细胞培养板,每孔500 μL,贴壁1 d后给药,每孔0.7 mL药液,样品共设20 μg·mL-1、8 μg·mL-1、3.2 μg·mL-1等3个浓度,每浓度3孔,以加等量DMSO的培养液代替药液的细胞为对照组,以8 μg·mL-1的拉米夫定为阳性对照。每3d换原浓度药液培养,6d后提取HBV DNA,经荧光定量PCR测定其DNA含量,根据测定结果计算样品对HepG2 2.2.15细胞DNA复制的抑制率[11],结果(见表1)。
表1目标化合物对HepG2 2.2.15细胞DNA复制的抑制率
编号抑制率(%)20(μg·mL-1)8(μg·mL-1)3.2(μg·mL-1)5a89.8131.7823.345b-41.27-38.1330.995c23.4644.8033.295d14.8848.8332.035e-37.12-8.8820.227a6.2334.5012.877b42.3237.3440.357c-7.4938.363.507d-11.83-10.6910.12 拉米夫定97.74
3 结果
通过化学方法合成了11个未见报道的马蹄金素双溴取代的衍生物,并对9个目标产物进行体外抗HBV活性筛选,结果显示,化合物5a、5c、5d、7b具有较好的抑制活性,其抑制率分别为89.81% (20 μg·mL-1)、44.80% (8 μg·mL-1)、48.83% (8 μg·mL-1)、42.32% (20 μg·mL-1)。
4 讨论
本研究合成了11个马蹄金素类似物,在制备化合物5a时,以1,4-二氧六环作为溶剂,外加无水碳酸钾质量10 %的水,所得产物的收率以及反应速率均比DMF作为溶剂的效果好,但以1,4-二氧六环作溶剂时,若没有加适量的水,则反应不发生。此外,还测定了9个衍生物的体外抗HBV活性,结果表明,所有化合物在低浓度时均有不同程度的抑制活性,当浓度增加以后,部分化合物显示出促进细胞生长的活性。化合物5a在20 μg·mL-1的浓度下具有较高的抑制率,达到89.81%,接近于拉米夫定的抑制率,该化合物具有进一步研究开发的价值。
[参考文献]
[1] Van Damme P, Zanetti A R, Shouval D, et al.Strategies for global prevention of hepatitis B virus infection[J].Adv Exp Med Biol,2010,659:175-188.
[2] Benhenda S, Cougot D, Buendia M A, et al.Hepatitis B virus X protein molecular functions and its role in virus life cycle and pathogenesis[J].Adv Cancer Res,2009,103:75-109.
[3] Azam F, Koulaouzidis A.Hepatitis B virus and hepatocarcinogenesis[J].Ann Hepatol,2008,7(2):125-129.
[4] Zoulim F.Hepatitis B virus resistance to antiviral drugs:where arewe going?[J].Liver Int,2011,31(1):111-116.
[5] Xu B,Huang Z, Liu C,et al.Synthesis and anti-hepatitis B virus activities of Matijing-Su derivatives[J].Bioorg Med Chem,2009,17(8):3118-3125.
[6] Qiu J, Xu B, Huang Z, et al.Synthesis and biological evaluation of Matijing-Su derivatives as potent anti-HBV agents[J].Bioorg Med Chem,2011,19(18):5352-5360.
[7] 梁光平, 曹佩雪, 杨秀虾, 等. NO型马蹄金素衍生物的合成及其初步的抗HBV活性[J].有机化学,2014,DOI:10.6023/cjoc201312003.
[8] 邱净英, 黄正明, 潘卫东, 等.马蹄金素衍生物的合成及抗乙肝病毒活性[J].中国药科大学学报,2012, 43(5):390-394.
[9]柴慧芳, 赵燕芳, 宫平.5-羟基-6-溴-1H-吲哚-3-羧酸酯类衍生物的合成及其抗乙肝病毒活性[J].贵州化工, 2008,33(4):20-23.
[10] 戴志群, 张炜炜, 王文清.1,5-二乙酰基-2,4-二氧六氢-1,3,5-三嗪糖苷的合成及抗病毒活性[J].化学世界,2009,(12):737-739.
[11] Korba B E,Gerin J L.Antisense oligonucleotides are effective inhibitors of hepatitis B virus replication in vitro[J].Antiviral Res,1995,28(3):225-242.

