内镜全层切除术治疗胃黏膜下小肿瘤的临床疗效分析
刘靖正, 任 重, 胡健卫, 秦文政, 钟芸诗, 周平红
(复旦大学附属中山医院内镜中心,上海 200032)
近年来,胃镜检查的数量逐年递增,胃黏膜下肿瘤的检出率明显增加[1-2]。既往外科手术是胃黏膜下肿瘤唯一的治疗方法[3]。近年来内镜技术的飞速发展及相关器械的不断研发,为内镜切除黏膜下肿瘤提供坚实的基础[4-5]。2009年,国内学者报道无腹腔镜辅助胃黏膜下肿瘤内镜全层切除术(endoscopic full thickness resection,EFTR)的临床研究[6-7]。EFTR技术促进内镜治疗的飞速发展,在临床上得到广泛应用。2015年1月至12月本院102例胃黏膜下小肿瘤(直径≤1 cm)病人行EFTR,取得良好的疗效。本研究进行回顾性分析。
材料与方法
一、一般资料
本研究胃黏膜下小肿瘤病人,男29例,女73例,平均年龄(57.01±10.41)(29~77)岁。内镜手术前常规完善超声内镜和CT检查,均为单发病灶,平均直径(0.68±0.25)(0.2~1.0)cm。肿瘤均位于胃底。起源于黏膜层6例,固有肌层96例。术前均告知家属和病人病情及手术风险,签署手术治疗知情同意书,并通过医院伦理委员会批准。
二、医疗器械
Olympus GIF-Q260J胃镜(日本 Olympus),GIF-2TQ260M双腔胃镜(日本Olympus),ERBE VIO-200D高频电切机(德国ERBE)和Hook刀(日本Olympus,KD-620LR)、IT 刀(日本 Olympus,KD-611L)、海博刀(德国ERBE),注射针(日本Olympus),APC氩气离子凝固器 (德国ERBE)、热活检钳 (日本Olympus,FD-430L),金属夹(南京微创),CO2注气泵(日本Olympus)。
三、术前准备
术前停用1周阿司匹林及其他抗血小板聚集药物、抗凝药物、解热镇痛药物和抗精神类药物。行常规血常规、凝血功能及心电图检查,进行术前评估。术前禁食、水8 h以上。
四、内镜操作
病人取左侧卧位,均气管插管全身麻醉。EFTR手术治疗过程如下:①生理盐水充分冲洗胃腔,胃镜下找到肿瘤,明确病灶所在部位(见图1A)。②Hook刀标记病灶,建议四点标记(见图1B)。③生理盐水+靛洋红(indigo carmine,靛胭脂)行黏膜下注射。本研究均为较小的黏膜下肿瘤,因此需严格控制黏膜下液体注射量,建议每标记点黏膜下注射量不超过1 mL。④病灶处黏膜抬举后,Hook刀切开病灶周围黏膜及黏膜下层,暴露瘤体后(见图1C),继续用Hook刀或IT刀分离,剥离至浆膜层。⑤全层切开胃壁浆膜层前,冲洗胃腔并吸净胃内液体,然后切穿浆膜层,尽量将瘤体推至胃腔内,完整切除(见图1D)。⑥创面缝合应用金属夹或金属夹及尼龙绳联合“荷包”缝合(见图 1E-F)。
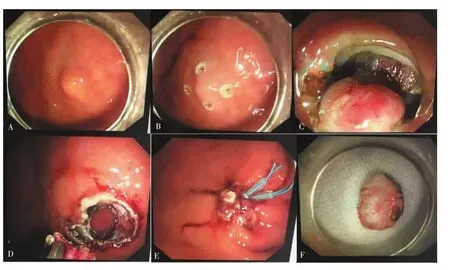
图1 EFTR治疗胃黏膜下小肿瘤
五、病理组织学检查及免疫组织化学检测
切除标本固定于中性甲醛溶液,立即送检。按照标本处理规范,完成标本切割及包埋切片。病理组织学检查包括肿瘤的大小(直径)、细胞类型等。免疫组织化学检测包括 CD34、CD117、DOG-1、SMA、DES、NES、S100、KI67。
六、术后处理及随访
术后常规放置胃管,行胃肠减压,禁食24~48 h。禁食期间给予静脉营养及质子泵抑制剂,应用抗生素预防感染。密切注意病人的生命体征及血常规等。术后3个月复查胃镜和超声内镜。
结 果
一、手术结果
102例均成功完成内镜治疗,肿瘤完全切除。平均手术时间(34.8±7.5)(11~126)min。术后病理检查结果肿瘤直径为 (0.50±0.36)(0.3~1.0)cm,肿瘤均位于胃底。
二、病理诊断结果
病理诊断结果如下:间质瘤51例(50.0%),均为G1期;平滑肌瘤45例 (44.1%);纤维瘤2例(2.0%);神经内分泌瘤2例 (2.0%);错构瘤1例(1.0%);淋巴瘤1例(1.0%),分型为黏膜相关淋巴组织的B细胞淋巴瘤。51例间质瘤病人免疫组织化学检测结果如下:CD34(+)、CD117(+)、DOG-1(+~++)、SMA(-)、DES(-)、NES(-)、S100(-)、KI67(2~3%),均为轻、中度异型和低危。
三、并发症发生情况
术中所有病人均出现不同程度气腹,术中常规应用腹腔穿刺针于右上腹穿刺排气。无病例发生术后腹腔出血、腹膜炎或腹腔脓肿症状。术后有12例出现体温升高,38℃~39℃,给予抗感染治疗后体温恢复正常。
四、随访情况
术后所有病人接受胃镜和超声内镜检查随访,无术后迟发性出血和穿孔,随访期间无肿瘤复发。
讨 论
胃黏膜下肿瘤胃镜下多表现为胃表面光滑的球形或半球形隆起性病变,常规胃镜活检无法获得病理学诊断。胃黏膜下肿瘤常见病理诊断类型包括平滑肌瘤、间质瘤、神经内分泌瘤、脂肪瘤、异位胰腺等[8]。临床常用超声内镜来初步判断黏膜下肿瘤的性质[9]。临床认为较大或伴有临床症状的黏膜下肿瘤需手术干预[10]。2010版NCCN指南[11]认为,直径>2 cm的间质瘤应手术治疗,<2 cm的间质瘤,超声内镜检查除外高危因素,可内镜随访。对于直径<1 cm的黏膜下肿瘤尚无定论。临床上病人因直径≤1 cm的黏膜下肿瘤反复接受胃镜及超声胃镜检查,给身心及经济带来很大负担。
对胃黏膜下肿瘤的内镜治疗术式选择,临床报道各有不同。除常规的内镜黏膜下剥离术外,还有一系列新技术的报道。刘靖正等[12]报道应用体外牙线牵引辅助EFTR治疗胃黏膜下肿瘤,96例均完整切除肿瘤,取得良好预后。李歆等[13]报道应用预荷包缝合技术治疗腔外生长型胃黏膜下肿瘤,15例均完整切除肿瘤,无严重并发症发生。王珊珊等[14]报道单钳道内镜下荷包缝合法封闭贲门及胃底黏膜下肿瘤EFTR后胃壁缺损的临床研究,32例缺损直径1~4 cm,均在胃黏膜下肿瘤切除术后成功缝合。现有临床研究证实了内镜治疗胃黏膜下肿瘤技术的可行性和安全性。
本研究针对不同层次的胃黏膜下小肿瘤,起源于黏膜下层6例,起源于固有肌层96例,采用EFTR,分析其安全性和可行性。102例均成功完成内镜治疗,肿瘤均完整切除。术后病理诊断结果包括间质瘤、平滑肌瘤、纤维瘤、神经内分泌瘤、错构瘤和淋巴瘤。本研究发现,胃黏膜下小肿瘤好发于胃底固有肌层,以间质瘤和平滑肌瘤为多。这与既往临床研究结论(位于胃固有肌层的多为间质瘤,少数肿瘤为平滑肌瘤)基本一致[15]。间质瘤起源于Cajal间质细胞,干细胞因子受体kit或血小板源性生长因子受体a基因突变所致[16]。临床研究发现,Cajal间质细胞多个受体中的一个位于胃底,可能与GIST好发于胃底有关[17],尚需进一步研究。
与传统外科手术相比,EFTR有创伤小、愈合快、住院时间短、费用低等优势。但发生出血和穿孔这两大并发症,是决定内镜治疗成败的关键。与胃窦、贲门处组织结构相比,胃底较薄,穿孔时有发生,且位置较难处理,需反复倒镜完成操作。因此,要求内镜医师有丰富的经验和娴熟的操作技能。
本研究总结,EFTR治疗中内镜医师应注意以下事项:①胃底肿瘤直径小,麻醉后出现肌肉松弛等,易出现无法找到肿瘤的情况。因此应做好标记,明确肿瘤部位。②操作时应层次清晰,发现血管,尽快提前处理,避免出血时盲目止血造成穿孔。术中出血时需用生理盐水冲洗创面。找到出血点后,应用切开刀电凝止血或热活检钳钳夹出血点,电凝止血。③剥离瘤体时应注意瘤体层次,保证完整切除肿瘤。④瘤体突出腔外或与浆膜层粘连时,应先吸净胃腔内的液体和气体,再做切穿浆膜层的主动穿孔,避免消化液外漏,造成腹腔感染。⑤术后胃创面处理应仔细,可用热活检钳烧灼止血,避免迟发性出血。⑥EFTR后,根据创面大小,可选用金属夹夹闭创面或金属夹及尼龙绳联合荷包缝合创面。在荷包缝合时,可用双腔镜完成,也可将尼龙绳固定于胃镜头端外侧或用金属夹固定尼龙绳,将其用胃镜送入胃内。⑦术中建议使用CO2,因其水溶性和脂溶性均远远高于空气,可明显减少病人术后腹胀等不适感[18]。
未来,随着内镜治疗技术的推陈出新,将有较多疾病不需外科手术来完成。

