“素养为本”的微项目教学在高中化学实验中的应用
史培艳

摘要:以二氧化硫制备、性质验证、喷泉实验的一体化、封闭式实验项目为例,开展“素养为本”的微项目教学,发展学生科学探究与创新意识、证据推理与模型认知素养;通过子项目问题交流讨论,培养学生化学符号表征及化学进阶思维能力。
关键词:素养为本;微项目教学;高中化学实验;二氧化硫
文章编号:1008-0546(2021)02-0093-05 中图分类号:G632.41 文献标识码:B
doi:10.3969/j.issn.1008-0546.2021.02.023
一、问题的提出
“素养为本”的化学课堂教学,以真实情境为载体,开设实验为主的多种探究活动,重视教学内容的结构化,改变学生的学习方式,注重学生实践、创新能力的培养。微项目教学是以学生为中心,以微型项目为载体,在真实情境中开展一系列探究活动的教学形式。微项目教学是实施化学课程,发展学生化学学科核心素养,体现学生个性化的一种新教学方式,具有项目式教学和微课的特点。微项目教学从学生的生活经验人手,依据学生的认知规律和最近发展区,创设真实生产、生活情境,融合专业知识和技能,提升学生解决实际问题、综合实践应用能力。
在科技抗疫的今天,国家重点组建实验室体系,实现产学研融通创新。农村学校的实验室仪器和药品陈旧,有的甚至不能使用,更缺乏现代化、数字化实验仪器。陈旧的实验器材阻碍不了教师和学生创新之举,借助乡土素材,融合化学知识,助推实验创新,提升实践技能。
“二氧化硫的性质与应用”上课前,需要提前制备二氧化硫并把二氧化硫通入水中制得二氧化硫的水溶液。进行实验探究过程中,二氧化硫的水溶液不穩定,会释放出具有刺激性气味、有毒的二氧化硫气体,导致学生对实验的兴趣削减。为了减少以上弊端,采用微项目教学,设计二氧化硫制备与性质的一体化、封闭式实验,促进学生对“含硫化合物的性质”的深度学习,提升学生化学学科核心素养。
二、微项目内容主题分析
1.教材分析
“二氧化硫的性质和应用”是苏教版《化学(必修第一册)》专题4第一单元第一课时内容。本单元在学习了物质的分类、物质的量浓度、氧化还原反应、离子反应等基础上学习二氧化硫制备与性质、含硫物质间转化、硫酸型酸雨成因与防治。根据结构决定性质,性质决定用途这一知识主线,进行有意义二氧化硫知识建构。二氧化硫是酸性氧化物,具有酸性氧化物通性;二氧化硫中硫的化合价为+4价,介于最低价一2价和最高价+6价之间,即有还原性也有氧化性;二氧化硫的特性为漂白性。通过设计实验方案、改进实验装置,进行二氧化硫实验分组合作探究,并绘制含硫物质之间转化的价类二维图。利用价类二维图促使学生内化氧化还原和物质分类等核心概念。
2.学情分析
学生已经具有分类观,理解氧化还原反应、离子反应大概念,掌握常见气体制备、一定物质的量浓度溶液的配制等,能设计气体制备及性质探究的实验方案并实施实验方案,观察现象,得出实验结论,也能用相关原理分析陌生情境问题和解决问题。学生已经知道二氧化硫是酸性氧化物,具有氧化性、还原性、漂白性;学生不了解不同酸碱指示剂变色范围和氧化还原反应的先后顺序原因。
3.教学策略
基于学生元认知、生活经验、最近发展区,给学生提供仪器和药品、文献,组织学生阅读课本和文献。学生借助身边的生活素材,在他人对二氧化硫性质改进成果基础上进行创新。受新冠病毒形状启发,设计多彩新冠模型变色实验。学生分组、分工、合作探究,展示成果并讲解各组设计实验方案、实验过程、实验现象、实验结论及实验注意问题。
4.专业拓展
利用不同酸碱指示剂不同变色范围(表1),探究二氧化硫与碱、盐溶液的变色反应。配制约0.1mol/L碱、盐溶液,并用精密pH试纸测其pH值(表2)。
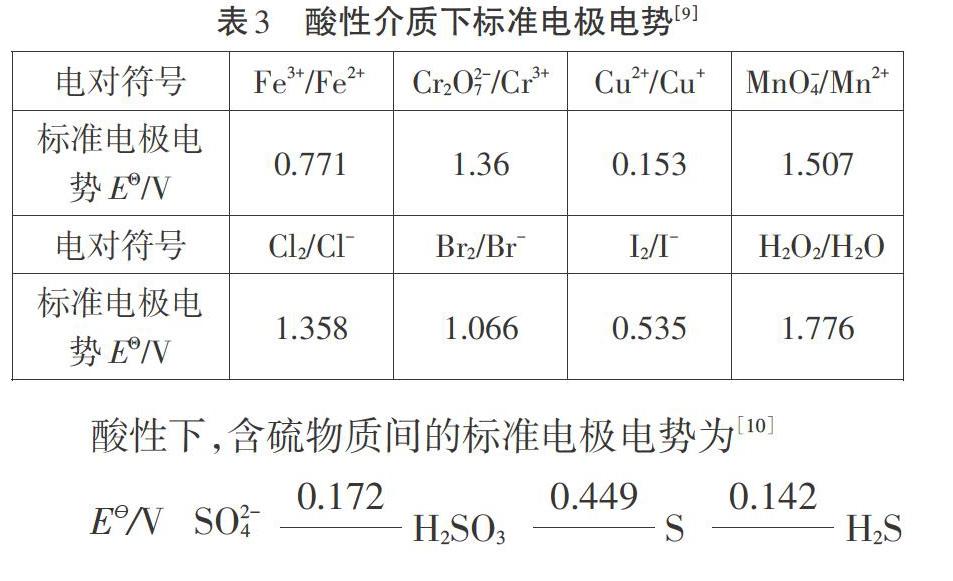
二氧化硫以还原性为主,与常见氧化剂反应的变色顺序是不同的,取决于氧化剂的氧化性强弱。通过文献查阅,298K时标准电极电势(表3),判断氧化还原反应的难易程度。
三、微项目教学目标
1.通过改进实验实现二氧化硫制备与性质的一体化,通过动手实验、观察、分析实验现象,收集实验证据,得出实验结论,发展学生证据推理与模型认知素养。
2.能从物质类别、元素价态的角度,认识物质转化路径,能用化学符号表征物质的转化,发展学生变化观念。
3.基于“绿色化学”理念设计实验方案,并对实验进行评价和优化,发展学生科学探究与创新意识、科学态度与社会责任素养。
四、微项目任务及教学流程
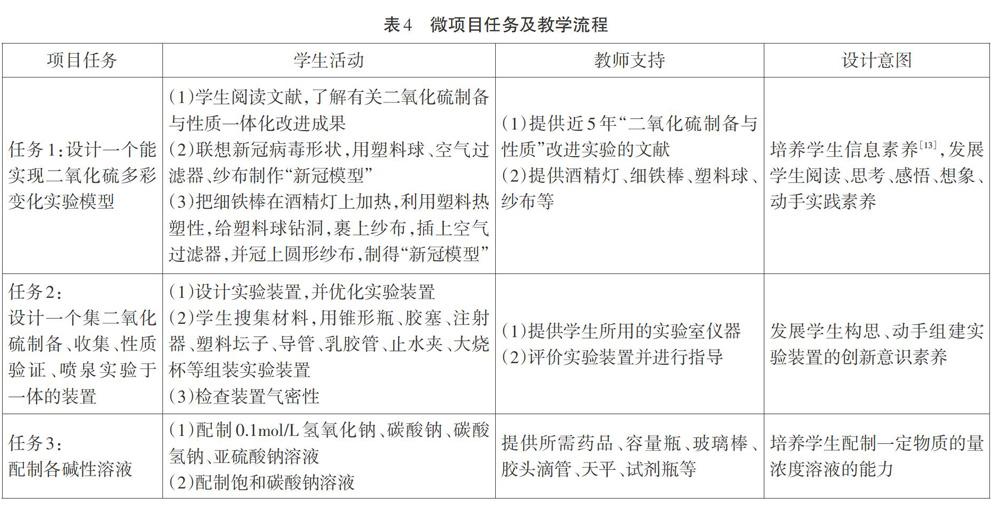
学生分组、分任务合作实验,其中1-6任务(表4)课前完成。
五、微项目实施过程及学生学习成果
1.展示学生课前任务成果把学生课前任务成果(图1)汇总,并展示给学生
观看。
实验装置如图2:塑料坛子中A、B是两个空心塑料球,塑料球上插入几个空气过滤器(类似冠),这样形成冠状病毒形状。A、B球用纱布包上,各“冠”上冠有纱布。A球纱布浸有NaOH溶液(酚酞),A球“冠”上的纱布按顺时针顺序分别浸有Na2CO3溶液(中性红)、NaHCO3溶液(甲基红)、Na2SO3溶液(溴甲酚绿与甲基红3:1混合)、饱和Na2CO3溶液(溴百里香酚蓝)、紫色石蕊、Na2S溶液、品红溶液(A7在最上方,检验二氧化硫是否收集满);B球纱布浸有FeCl3(KSCN)溶液,B球“冠”上的棉花按顺时针顺序分别K2Cr2O7溶液、FeCl3溶液、CuClz溶液、12/淀粉溶液、酸性KMnO4溶液、广泛pH试纸(水湿);A、B形成多彩的“新冠模型”。塑料小坛子中导管上粘有双氧水和氯化钡溶液浸湿的广泛pH试纸。
2.实验过程
实验过程如表5及图3所示。
3.实验现象变化原因分析
学生分组、合作讨论实验现象变化的原因。
子任务1:两处品红溶液颜色变化慢、快原因。
学生成果:亚硫酸钠与75%硫酸溶液反应是放热反应,生成热的二氧化硫气体,热的二氧化硫气体难能使品红溶液褪色;二氧化硫经导管进入塑料坛中,经冷却,易使品红溶液褪色;导管中是浸有品红的棉花,成团状,二氧化硫与品红接触面较小,而塑料坛中是浸有品红的单层纱布,成片状,二氧化硫与品红接触面大,后者反应速率快,褪色快。
子任务2:二氧化硫与同浓度不同溶液反应颜色变化快慢原因(A新冠模型)
学生成果:二氧化硫使紫色石蕊变红,说明二氧化硫是酸性氧化物,与水反应生成亚硫酸。0.1mol/LNaOH、Na2CO3、NaHCO3、Na2SO3溶液pH分别为13.0、11.6、8.3、10.0,碱性不同,c(OH-)大小不同,二氧化硫与它们反应本质是与OH-反应,c(OH-)大的反应快,颜色变化快。
子任务3:二氧化硫与同浓度不同氧化剂变色快慢不同原因(B新冠模型)
学生成果:同浓度不同氧化剂的标准电极电势不同,电极电势越大,其氧化性越强,与二氧化硫反应就越快。
子任务4:二氧化硫分别使酸性高锰酸钾溶液、品红溶液褪色原理相同吗?
学生成果:不同,二氧化硫与酸性高锰酸钾溶液因发生氧化还原反应而使之褪色,二氧化硫与水反应生成亚硫酸,亚硫酸与品红结合为不稳定无色物质,前者利用二氧化硫的还原性,后者利用二氧化硫的漂白性。
子任务5:两处广泛pH试纸变红程度不同原因
B6冠上广泛pH试纸呈红色,是因为SO2+H2O=H2SO3=H+HSO3-导管上广泛pH试纸呈红色且颜色深,是因為H2O2+SO2=H2SO4;H2SO3为弱酸,H2SPO4是强酸,酸性不同,广泛pH试纸红色深度不同。
子任务6:烧杯中是蓝色溶液,为什么形成黄色喷泉呢?
学生成果:打开止水夹b,多余二氧化硫与氢氧化钠溶液作用,c(OH-)减小,pH减小。溴百里香酚蓝变色pH范围是6.2-7.6,颜色变化为黄一绿一蓝。溶液由蓝变绿,再变黄,说明二氧化硫稍过量。向锥形瓶中加水,止水夹a是打开状态,整个装置是相通的,二氧化硫因溶于水且部分被挤压入氢氧化钠溶液导致装置内压强减小,外压大,形成黄色喷泉。
子任务7:通过实验现象说明含硫物质之间具有怎样的关系?
学生成果:同种价态含硫物质之间、不同价态的含硫物质之间能相互转化,如图4价-类二维关系。
五、微项目教学反思及改进建议
1.以学生为主体,教师为主导
微项目教学过程中,教师为主导,是组织者、指导者、点拨者;学生为主体,是亲历者、体验者、探究者。整个过程中,学生通过项目,动手实验体验知识的产生过程。教师为学生提供活动的场所、空间、材料,适时针对学生存在的问题进行指导。
2.以学定项,难易适中
选择的项目不仅符合课程标准要求,还要适合学情,根据学生的认知规律及最近发展区选择难易适度的项目。过难的项目,学生很难完成,会产生挫败感,兴趣降低;过易的项目,学生容易完成,没有挑战性,不能激发学生潜力。适中的项目,学生既有挑战性又能完成,有成就感和自豪感,乐意去做,能发挥学生内在动力。
3.利于学生学科核心素养发展
在真实情境中解决真问题,利于学生科学探究、宏观辨识、微观探析、变化观念等素养的发展,利于学生化学思维能力的培养,利于学生完成任务共同体意识的强化。
4.存在问题及改进建议
乡村中学班级人数多,分组合作时,有的学生不积极参加微项目学习;乡村中学实验药品较久,失效,导致有的实验现象不明显;实验室没有网络,不能及时、适时搜索资料等。改进建议:教学小班化、网络化、微型化;资源时代化、更新化、跟进化。

